Пошаговая инструкция по аффинажу золота дома и в лаборатории
Аффинаж золота – это процесс очистки жёлтого драгоценного металла от различных примесей, в результате проведения которого предполагается возможным получение чистого драгметалла. Аффинаж золота можно проводить в домашних и лабораторных условиях. Специфика и особенности этого процесса зависят от способов и места его проведения. Мы предлагаем вам ознакомиться с альтернативными способами аффинажа золота в домашних и лабораторных условиях.
Способы
Аффинированное золото
Получить аффинированное (чистое) золото можно электролитическим или химическим способом. В ювелирном производстве, как правило, используют химический способ аффинажа ввиду того, что целесообразность применения электролитического способа проявляется исключительно при больших объёмах драгметалла и регулярном применении, то есть на больших производствах.
В целом, специалисты обычно называют три альтернативных способа очистки золота от примесей:
- мокрый (химический);
- сухой (обработка хлором);
- электролитический.
Химический способ рассчитан исключительно на переработку тех благородных металлов (в том числе и золота), примеси которых могут содержать в себе не только другие металлы, но и их соединения или же природные сплавы.
Выбор способа и метода аффинажа золота главным образом зависит от состава сплава или соединения.
Если в составе сплава содержится большое количество серебра, которое, как известно, препятствует его растворению в царской водке, образуя нерастворимый слой в кислоте, в такой сплав обыкновенно в качестве «разрыхлителя» добавляют медь.
Важно, чтобы процентное содержание серебра в таком сплаве составляло не менее пяти процентов всей его массы.
После этого компоненты растворяют в азотной кислоте, которая помогает удалить нежелательные частицы серебра, а металлы, которые выпали в осадок, окисляют посредством использования царской водки, после чего восстанавливают их. В случае с золотом таким восстановителем будет хлорид олова.
Аффинаж золота посредством использования хлора заключается в измельчении сплава металла до порошка и пропускании газообразного хлора через этот нагретый порошок. Результатом этой реакции является следующее: образуется соль металла (в случае с золотом – хлорид золота).
Если в примеси содержатся другие металлы, то вам важно знать следующее: при высоком нагревании хлорид серебра концентрируется в верхней части, а соли других металлов находятся ниже.
Электролитический способ заключается в осаждении драгметаллов на электроде. Он включает в себя два этапа:
- Растворение одного из электродов в царской водке или соляной кислоте, которое происходит под действием тока.
- Осаждение драгметаллов на втором электроде, которое происходит в виде слоёв, первый из которых будет представлять самый благородный металл.
Для получения золота электролитическим аффинажем необходимо использовать золото пробы не ниже 950. Только из такого материала в результате можно получить Fine Gold 999,9 пробы.
О других способах аффинажа золота в домашних и лабораторных условиях мы расскажем в деталях ниже.
С использованием цинка
Золотая капля крупным планом
Для того чтобы очистить золото от примесей первоначально его необходимо смешать с цинком. Для проведения данной операции потребуются следующие инструменты:
- тигель;
- большой и прочный пинцет;
- стальная спица;
- титановая палочка толщиной два-три миллиметра;
- колба из огнеупорного стекла;
- электрическая плита;
- колпак с отверстием на дне;
- аппарат для плавки металла.
Материалы, которые необходимы для проведения аффинажа:
- Чистая бура (в идеале – аптечная).
- Азотная кислота (65-70%).
- Соляная кислота (36-38%).
- Цинк-разрыхлитель.
Это важно! На каждые десять грамм золотого лома необходимо использовать десять грамм цинка.
Изначально тигель необходимо просушить и раскалить на электроплите. После этого в углубление тигеля добавляем буру. С помощью пинцета опускаем лом в тигель и нагреваем до покраснения. Следующим этапом посыпаем лом щепоткой буры.
Температура плавки должна соответствовать следующей:
- 999 проба – 1068 градусов по Цельсию;
- сплавы с серебром и медью 500 и ниже пробы – 900 градусов по Цельсию.
После полного расплавления золота и образования жидкого шарика добавляем маленькие кусочки цинка, оптимальный размер которых 6х6х6 миллиметров. Добавлять следующий кусочек цинка можно только тогда, когда растворится предыдущий.
Полученный таким образом сплав необходимо размельчить в ступке, предварительно накрыв её материей.
Полученный таким образом порошок необходимо поместить в стеклянную колбу и поставить её на электроплиту. В колбу залить шестьдесят-семьдесят миллилитров концентрированной азотной кислоты. Когда пройдёт реакция, следует добавить ещё сорок-пятьдесят миллилитров кислоты. Процедуру повторить два-три раза.
Это важно! Общий объём кислоты не должен превышать двести миллилитров.
После того, как пройдёт реакция, колбу с раствором необходимо установить на плиту и довести до кипения на медленном огне.
Далее – промываем осадок с помощью добавления в остывший раствор в колбе чистой холодной воды, объём которой должен составлять половину объёма колбы. Раствор взболтать и дождаться оседания хлопьев золота на дно. Жидкость аккуратно слить так, чтобы осадок остался в колбе. Осадок промывать до тех пор, пока вода с осадком не станет прозрачной.
Вместе с осадком оставляем в колбе небольшое количество воды. Берём глубокую посудину, застилаем её дно марлей, и выливаем остаток в посуду. Осадок, оставшийся на марле, обильно посыпаем бурой, завязываем в тугой узелок, промокаем фильтровальной бумагой, и помещаем в тигель.
Узел и тигель вновь посыпаем бурой и помещаем на электроплиту, тигель накрываем колпаком. Греть необходимо до тех пор, пока марля не истлеет, а бура не расплавится. Осадок склеится в небольшой ком, после чего можно снять колпак и плавить золото. В результате должен образоваться красный шарик на дне тигля.
Прекращать процесс можно только тогда, если при прекращении нагревания золото начинает затвердевать в течение нескольких секунд, а его поверхность становиться чистой и блестящей.
Затвердевший на дне тигля металл необходимо сразу достать, очисть от буры прокипятив в растворе отбела, состав которого следующий:
- пол-литра воды;
- десять миллилитров азотной кислоты;
- двадцать миллилитров соляной кислоты.
Время кипячения – пять минут в колбе.
Слиток ополаскиваем в чистой воде.
Электролиз
Электролитический способ аффинажа золота в наше время – самый простой и эффективный.
Для его применения необходимо наполнить большую ванну смесью хлорного золота и соляной кислоты.
Аноды электролитических ванн в процессе такого аффинажа отливаются из требующего очистки золота, а катоды образуются из специальной волокнистой золотой жести.
Электрохимическая реакция происходит за счёт подачи напряжения в ванне на электроды, благодаря чему на жести оседает чистое золото, проба которого часто достигает 999,9.
В процессе такого аффинажа на дне ванны образуется шлам, который содержит в себе все дополнительные примеси, которые были в сплаве до начала процесса.
Железный купорос
Золото в «царской водке»
Если золото в изделии представляет собой хлорид жёлтого драгметалла, который растворён в «царской водке», для аффинажа такого изделия необходимо использовать раствор сернокислого железа.
Сульфат железа растворяют в воде, пропорции сульфата и воды следующие: один к двум. Если раствор помутнел (это связано с происходящим процессом окисления) в раствор необходимо поместить чистые железные гвозди. Пропорции следующие: пять грамм гвоздей на сто грамм раствора.
Первый этап аффинажа заключается в испарении избытка азотной кислоты под вытяжным колпаком. Для этого «царскую водку» в совокупности с хлоридом золота необходимо нагреть в фарфоровой чаше с добавлением хлорида натрия, который поможет предотвратить распад хлорид золота.
Между такой чашкой и открытым огнём необходимо поместить железную сетку с асбестовым покрытием. Раствор в процессе нагревания необходимо помешивать стеклянной палочкой и попеременно добавлять в него небольшое количество соляной кислоты.
Это важно! Необходимо добиться загустевания жидкости до сиропообразного состояния, после чего её необходимо остудить. Когда жидкость остынет, нужно добавить соляную кислоту и отфильтровать жидкость.
К фильтрату добавляют насыщенный раствор сульфата железа. Благодаря таким манипуляциям золото выпадет в осадок и приобретёт вид красно-коричневого тяжёлого порошка, образовавшегося на дне сосуда.
Такой осадок также необходимо отфильтровать, промыть водой и собрать на бумажном фильтре, который впоследствии сжечь. Полученный таким образом металл – ни что иное как чистое золото.
Правильность проведения всех описанных манипуляций гарантирует получение чистого золота наивысшей пробы.
Хлорное олово
Химический процесс аффинажа золота
Уникальность процесса аффинажа с использованием хлорного олова заключается в том, что он:
- простой в применении;
- не вреден для здоровья;
- в осадок выпадает только золото.
Сам процесс заключается в следующем:
Необходимо взять порошок хлорного олова, к которому добавить одну часть воды и одну часть соляной кислоты.
В золотосодержащий раствор необходимо добавить хлорное олово. При наличии золота – произойдёт реакция.
Если реакция произошла, раствор необходимо оставить на двенадцать-двадцать четыре часа.
Осадок выпадет на дно. Его необходимо прокипятить в соляной кислоте, благодаря чему он приобретёт желтоватый окрас.
Более детально процесс описан на видео, представленном ниже.
Сущность аффинажа
Процесс аффинажа золота не такой сложный по своей сущности, как может показаться на первый взгляд.
Его довольно просто проделать не только в лабораторных условиях и с наличием специальных знаний, но и дома, имея под рукой минимум реагентов.
Получить чистое золото можно следуя подробным инструкциям, которые были представлены в этой статье.
2015-02-27
Источник: https://siqnalrp.ru/stati-o-dragocennyh-metallah/90544-poshagovaya-instruktsiya-po-affinazhu-zolota-doma-v-laboratorii.html
Как растворить золото: обзор химикатов, способных растворить благородный металл
Иногда у рядового обывателя появляется желание отделить золото от различных примесей. На первый взгляд, растворение золота (а без этого его просто не выделить) процедура достаточно трудоемкая, но осуществимая, нужно лишь знать, какими ингредиентами можно пользоваться, а какими нельзя.
Чем растворить золото?
Процесс извлечения чистого золота через его растворение может осуществляться различными способами. Некоторые его получают путем цианирования.
Под цианированием следует понимать процедуру извлечения посредством цианистого калия. Другие используют для отделения фтор.
Следует заметить, что эта процедура очень опасная. Дело в том, что процесс осуществим лишь на чрезвычайно высоких температурах. Кроме того, фтор относится к одним из самых ядовитых веществ в природе.
Самым популярным способом считается растворение золота при помощи «царской водки». Примечательно то, что «царская водка» применяется в этой сфере с 1270, а в России, с 1742 года, и до сих пор эта методика является безусловным лидером.
Также, если появилась потребность из обычного золота 585 пробы сделать 999, «царская водка» и здесь окажется незаменимым помощником.
Что потребуется для процесса и за счёт чего металл растворяется?
Прежде чем приступить к непосредственной процедуре, следует знать, как растворить золото. Также необходимо заранее подготовить:
- Азотную кислоту.
- Серную кислоту. Оба компонента должны быть концентрированными.
- Ёмкость для реакций. Для этого лучше всего подойдет обычный стакан из лаборатории или стеклянная колба.
- И главный участник процесса – ювелирный лом, либо любая другая деталь с элементами драгоценного металла.
Многие удивляются, как так происходит, что смесь кислот растворяет царя металлов. На самом деле при соединении двух видов кислот и драгоценного металла, появляется новый продукт.
Вас может заинтересовать: Белое золото и серебро: как отличить?
Называется он тетрахлораурат водорода, или если по иному — золотохлористоводородная кислота.
Сам процесс реакции происходит следующим образом — Au + HNO3 + 4 HCl = HAuCl4 + NO + 2 H2O.
Это своеобразное уравнение дает объективно понять, что для процесса растворения 1 гр.
Драг металла потребуется не менее 5 мл реактивной жидкости. Что самое интересное, в качестве растворителя выступает не азотная кислота, а серная.
Азотная кислота в данном случае требуется лишь для того чтобы выступить в роли катализатора.
Как по шагам растворить золотое изделие?
Первым делом, если в качестве материала выступает лом драг металла, либо изделия с примесями, следует провести очистку посредством феромагнитного вмешательства.
Далее процесс продолжается в виде обработки чистой азотной, либо других кислот. Только после этого можно приступать к непосредственному растворению.
Начинать следует с точных замеров пропорций. То есть, если в потенциальном материале масса равняется 1 грамму, следует приготовить 3.75 миллилитров концентрированной соляной кислоты, после чего все смешать в таре.
Практически сразу после смешивания должны наступить растворяемые процессы. Как только реакция завершится, раствор сливается и повторяется как в первом случае.
После добавления 2 порции соляной кислоты, колбу необходимо подвергнуть нагреву. В процессе нагрева не спеша вносится следующая составляющая в виде азотной кислоты.
Если изначальное соотношение кислот равняется 3 к 1, то на 1 грамм металла понадобится 1.25 мл азотной кислоты и ни в коем случае не больше, так как в следующем этапе ее будет сложно выделить.
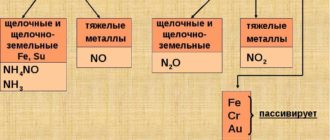
В течение короткого времени драгоценный металл полностью растворится, но следует заметить, под определением полностью имеется ввиду исключительно золотая составляющая. Другие составляющие, например, серебряные имеют свойство пассивироваться.
Как только весь процесс подошел к стадии завершения, следует выждать 20-30 минут, поддерживая температуру нагрева на прежнем уровне.
Одно маленькое, но важное замечание! Мало знать в чём растворяют золото, необходимо следовать чётким рекомендациям и обязательно соблюдать технику безопасности.
Ни в коем случае при нагреве не следует допускать процесса кипения. Если это произойдет, драг металл начнет выпадать в осадок раньше времени, а это значительно осложнит дальнейший этап осаждения аурума в чистом виде.
Источник: http://VseoZolote.ru/interesno/kak-rastvorit-zoloto.html
Аффинаж золота в домашних условиях: получаем чистый металл из радиодеталей и микросхем разными способами
Аффинажем называется очистка металла от примесей.
Этот процесс состоит из ряда последовательных процессов отделения лишних компонентов физическими и химическими способами.
Некоторые из методов аффинажа, применяемые в промышленности, можно реализовать и в домашних условиях, однако порой затраты на осуществление реакций превосходят прибыль от полученного благородного металла.
В данной статье мы расскажем, как снять и отделить золото от радиодеталей и достать его из микросхем, как сделать это безопасно своими руками.
Где содержится данный драгоценный металл?
Сотни тонн золота ежегодно используются при производстве радиодеталей и компьютерных микросхем. Контакты из этого металла отличаются высокой электропроводимостью, они не подвержены окислению, поэтому нашли широкое применение.
Золото содержится в следующих компонентах:
- диодах;
- транзисторах;
- стеклянных электродах;
- реле;
- портах;
- перемычках;
- модулях памяти материнских плат.
Отметим, что на практике в радиодеталях золота может быть гораздо меньше, чем должно быть по документам (особенно в технической продукции, сделанной после 1989 года).
Способы очистки от примесей
Основной способ выделения чистого металла из смесей, в том числе из различных радиодеталей, заключается в химическом рафинировании. Очень распространено растворение в царской водке (смеси азотной и соляной кислоты) с последующим пропусканием через фильтр и восстановлением.
Метод электролиза
При методе электролиза золото из радиодеталей или любое другое, подвергнутое воздействию серной или соляной кислоты, осаждается на катоде при прохождении через раствор электрического тока.
В промышленности применяют катод из уже очищенного золота, дома можно использовать железный или свинцовый.
Падение силы тока – сигнал, что процесс растворения завершен. Данный метод также является действенным и поэтому достаточно распространенным.
Для вытравливания золота с поверхности радиодеталей применяют самый обычный аптечный раствор Люголя – он представляет собой смесь йода и йодида калия. В процессе реакции образуются комплексные анионы, содержащие молекулы золота.
Для увеличения скорости химики добавляют серную или азотную кислоту. Процесс растворения может продолжаться сутками.В дальнейшем благородный металл осаждается из раствора разными способами.
Использование отбеливателя «Белизна»
Популярный бытовой отбеливатель состоит преимущественно из гипохлорида натрия.
Это вещество в смеси с соляной кислотой позволяет получить хлор, который в дальнейшем используют для растворения золота с образованием хлорида золота.
После этого в раствор добавляют бисульфат натрия.
По окончании реакции на дне сосуда остаются серые частицы – это и есть золото, которое приобретет естественный цвет после переплавки.
Другой вариант – смешать «Белизну», столовую соль (хлорид натрия) и аккумуляторный электролит, которые представляет собой не что иное, как серную кислоту. Полученная при реакции хлорноватистая кислота растворяет золото – его в дальнейшем нужно восстановить.
Аффинаж «без кислоты»
Распространенные в интернете рецепты получения из радиодеталей и растворения золота «без кислоты» по сути вводят читателей в заблуждение, поскольку кислота (обычно соляная) образуется в результате реакции других веществ.
Кроме того, не все знают о том, что применяемый в подобных случаях аккумуляторный электролит также является кислотой.
Использование перекиси водорода
Извлечение золота из радиодеталей перекисью водорода осуществляется следующим образом.
Данное вещество, по-другому именуемое пергидролем, реагирует с соляной кислотой, растворяя золото. Для этого золотосодержащее сырье заливают кислотой и добавляют перекись.
Образовавшаяся золотохлористоводородная кислота в дальнейшем разлагается на элементы.
Для этого можно использовать термический способ (направить на вещество синее пламя горелки) либо химический. Последний состоит в восстановлении золота путем добавления сульфата железа.
Другие методы извлечения
Существует множество других способов аффинажа, которыми можно собрать золото с микросхем, например, электролитом и аммиачной селитрой.
В данном случае электролит смешивается с аммиачной селитрой – так называется соль азотной кислоты. Полученный состав способен растворить благородный металл.
Большая часть других способов также основана на растворении золота и его последующем восстановлении.
Процессы различаются по:
- стоимости;
- доступности компонентов;
- скорости реакции.
Пошаговая инструкция добычи металла из радиодеталей и микросхем
Для извлечения золота из микросхем и радиодеталей целесообразно воспользоваться царской водкой.
Чтобы аффинировать золото данным способом необходимо осуществить действия в указанной ниже последовательности:
- измельчить компоненты механическим путем, отделив части, в которых содержится золото;
- избавиться от органических веществ путем обжигания или прокаливания;
- открыть в помещении окна для лучшего проветривания;
- для экспериментов приготовить сосуд из боросиликатного стекла;
- заготовки поместить в концентрированную смесь 36% соляной (3 части) и 95% азотной кислоты (1 часть) небольшими порциями – до 3 грамм за раз, на 100 г сырья потребуется 500 мл царской водки;
- раствор нагреть при постепенном доливании азотной кислоты;
- наличие золота проверить хлоридом олова;
- раствор отфильтровать, затем из него удалить азотную кислоту.
В дальнейшем золото может быть восстановлено с помощью железного купороса, пергидроля, щавелевой кислоты или сульфата гидразина. Полученное золото переплавляется в слиток с использованием тигля.
Отметим, что в домашних условиях заниматься очисткой золота небезопасно из-за значительной едкости и токсичности используемых веществ и выделяющихся летучих соединений.
Кроме того, потребуются углубленные познания в химии.
Полученный в результате очистки золотой слиток (королёк) чаще всего имеет незначительный вес. Однако даже в таком количестве он представляет интерес для скупщиков.
Объявления о покупке золота можно без труда найти в интернете или местных газетах.
Зачастую цельный металл приобретают те же фирмы, что занимаются скупкой радиодеталей.
Золотом могут заинтересоваться и скупщики других металлов (например, алюминия или латуни).
Если покупатель находится в одном городе с продавцом, сделка совершается при визите по указанному адресу.
Скупщик сам взвешивает металл и проверяет его качество, после чего назначает цену. Разумеется, если есть возможность, желательно проверить все предложения на рынке, чтобы выбрать самое выгодное. В другой город слиток можно отправить по почте наложенным платежом.
Некоторые ломбарды также готовы принять товар такого рода. Чтобы выяснить, по какой цене заведение готово будет приобрести золото, обратитесь к работнику ломбарда. Другой вариант – самому подать объявление. В этом случае вам лишь придется ждать звонка от потенциального покупателя.
Если заниматься аффинажем в промышленных масштабах, то следует опираться на действующие законы.
Чтобы легально заниматься оборотом драгоценных металлов, нужно зарегистрироваться в качестве ИП или создать ООО.
При сбыте золота ориентируйтесь на его чистоту и на рыночную стоимость.
Цена за грамм драгметалла 999 пробы устанавливается Центробанком России. С 2004 года цены на него непрерывно растут. Самый значительный скачок наблюдался в 2016 году, когда стоимость превысила 3 тысячи рублей за грамм.
Источник: https://rcycle.net/metally/dragotsennye/affinazh/poluchenie-zolota-v-domashnih-usloviyah-iz-radiodetalej-i-mikroshem
Очистка золота путём растворения в царской водке
Часто возникает необходимость очистить золото от других металлов, содержащихся в сплаве или в ломе. При получении золота путем цианирования, растворения руды в растворе цианистого калия, в конечном продукте золото также часто оказывается в смеси с серебром и медью.
При необходимости сделать из низкопробного золота высокопробное возникает та же задача — очистить драгметалл от сопутствующих примесей. Классический способ, позволяющий достаточно просто провести очистку, растворение золота в царской водке.
Оглавление
- 1 Растворение золота
- 2 Фильтрование раствора
- 3 Осаждение золота
Вернуться
Растворение золота
Самостоятельно приготовленная смесь
Царская водка, или Aqua Regia, это смесь концентрированных азотной и соляной кислот в соотношении 1:3 по объему и примерно 1:2 по массе. Если точнее, 65-68% по массе азотной кислоты (HNO3) и 32-35% соляной кислоты (HCl).
Столь странное название этой смеси было дано алхимиками: только эта «водка» обладала способностью растворять «царя металлов» — золото (само слово «водка» в русском научном языке обозначало химическую «воду» — жидкий реактив; за крепким алкогольным напитком этот термин закрепился уже намного позже).
В результате реакции металлического золота с царской водкой образуется комплексное соединение — золотохлористоводородная кислота, или тетрахлораурат водорода. При этом происходит следующая реакция:
Au + HNO3 + 4 HCl = HAuCl4 + NO + 2 H2O.
Исходя из данного химического уравнения и плотности царской водки получается, что для растворения 1 грамма золота нужно минимум 5 мл реактива. При этом на самом деле растворяется золото только в соляной кислоте. Ни азот, ни кислород в состав золотохлористоводородной кислоты не входят. Азотная кислота выступает только как окислитель, катализирующий вступление золота в реакцию. В связи с этим процесс растворения лучше производить следующим образом.
Прежде всего, если мы имеем дело с содержащим золото ломом, нужно с помощью магнита удалить ферромагнитные частицы. После этого максимально очистить золото от примесей с помощью других кислот, прежде всего чистой азотной. Лишь затем можно начинать процесс растворения золота.
Сначала нужно отмерить по 3.75 мл соляной кислоты на каждый грамм золотосодержащего металла и залить его только ей одной. Если при этом начинается более-менее заметная реакция, значит, какие-то примеси уже начали растворяться. Нужно дождаться окончания процесса, слить раствор и залить металл новой порцией соляной кислоты. Теперь нужно начать подогревать емкость с реактивом, понемногу добавляя азотную кислоту из расчета 1.25 мл на 1 грамм металла.
Главное — не переборщить с азотной кислотой, так как при осаждении золота из раствора именно от нее нужно будет наиболее последовательно избавляться. Как только весь металл растворится, следует сразу же перестать добавлять ее в раствор.
Притом не обязательно растворится все исходное вещество: серебро, в отличие от золота, в царской водке пассивируется за счет образования плотной хлоридной пленки на поверхности.
После того как растворение закончилось, следует продержать раствор нагретым около получаса.
Вернуться
Фильтрование раствора
Теперь настало время отфильтровать раствор. Пока фильтр можно использовать достаточно грубый, а более тонкая очистка произойдет позже.
Полученный в результате осадок
Следует понимать, что сама по себе царская водка — вещество достаточно неустойчивое: соляная и азотная кислоты вступают в реакцию между собой. Изначально прозрачная, она вскоре окрашивается в оранжево-буроватый оттенок оксидов азота, а потом и вовсе теряет окислительные свойства. При этом происходят следующие реакции:
HNO3 + 3 HCl = 2Cl + NOCl + 2H2O
NOCl = NO + Cl
2NO + O2 = 2NO2
Кроме того, обе кислоты просто испаряются. В связи с этим, целесообразно на этой стадии выдержать раствор около суток, так как это облегчит дальнейший процесс выпаривания азотной кислоты.
При выпаривании следует добавить к раствору небольшое количество серной кислоты, не более 50 мл на литр. Это поможет осадить остаточные количества свинца и хлорида серебра (который, хоть и малорастворим, в небольших количествах в растворе может присутствовать). Кроме того, и процесс выпаривания пойдет быстрее.
Нагревание производится медленно и осторожно. Раствор упаривается до консистенции сиропа (не более!). До кипения доводить нельзя, так как в этом случае нельзя исключать выпадения золота в виде металлического осадка уже на этой стадии.
После добавляем к раствору соляную кислоту до исходного объема и снова упариваем до сиропообразного состояния. Процесс повторяется трижды. Следом за этим жидкость разбавляется в 2 раза холодной водой и оставляется в холоде на сутки.
При этом остатки хлорида серебра должны выпасть в осадок: он растворяется только в концентрированной соляной кислоте, и тем лучше, чем выше температура. Соответственно, при падении концентрации и температуры AgCl осаждается.
Вот теперь проводится фильтрование «по полной программе»: никакой мути в растворе остаться не должно.
Вернуться
Осаждение золота
Осаждение золота из раствора может производиться с помощью различных реактивов (перекись водорода, щавелевая кислота, сульфит или пиросульфит натрия), но обычно используется железный купорос — сульфат двухвалентного железа FeSO4. При этом происходит следующая реакция:
HAuCl4 + 3FeSO4 = Fe2(SO4)3 + FeCl3 + HCl + Au.
Железного купороса нужно брать не менее 13 г на 1 г предполагаемого конечного продукта. Достаточно развести сульфат железа теплой водой с небольшим количеством соляной кислоты и добавить в имеющийся раствор. При этом жидкость сразу должна помутнеть.
Если этого не происходит и особенно если начинается шипение, значит, азотная кислота не выпарена до конца.
В этом случае можно повторить процесс выпаривания, а можно просто добавить несколько больше сульфата железа (он хорош именно способностью легко и безопасно нейтрализовать избыток азотной кислоты).
Через сутки процесс осаждения завершается. Если при добавлении в раствор крупинки железного купороса не возникает облачка мути, значит, выделение золота завершилось. Если муть появляется, нужно добавить еще сульфата железа и подождать.
В последнюю очередь, после слива всего раствора, получившийся золотой осадок следует промыть соляной кислотой для очистки от солей железа, а потом — раствором аммиака (нашатырным спиртом) для удаления остатков меди.
Таким образом можно получить золото 999 пробы и даже выше. С ювелирной точки зрения такой металл будет соответствовать наивысшей пробе — 24 карата.
Источник: https://grammzolota.ru/dobycha/vyidelenie-osazhdenie-rastvorenie-tsarskoy-vodke.html
Как получить золото в домашних условиях? Секретные способы добычи
Даже само слово «золото» магически действует на человека, не говоря уже о его виде. Мечты о золотоносных реках и приисках пусть так и остаются мечтами. Однако для тех, кто все-таки хочет почувствовать себя золотодобытчиком, можно предложить вполне реальный путь – добыча золота в домашних условиях. Конечно, речь не идет о килограммах, но можно получить достаточное количество металла, чтобы использовать его в практических целях.
Свойства золота
Золото – это драгоценный металл, который широко применяется в ювелирных украшениях. Однако помимо ювелирной ценности надо отметить, что его уникальная электропроводность обуславливает применение в электронике, где в особоважных деталях надо обеспечить малое сопротивление при минимальных габаритах. Именно такие детали становятся основным сырьем для домашней золотодобычи.
При организации добычи и переработки золота следует учитывать его основные свойства:
- Большой удельный вес. Эта характеристика используется при реализации такой технологии, как промывка, когда большой вес заставляет оседать золотые крупицы.
- Высокая пластичность, облегчающая ковку металла при изготовлении из него украшений. Из золота можно изготавливать очень тонкие нити.
- Инертность. Золото не вступает в химическую реакцию с большинством известных кислот, щелочей и растворителей. Только «царская водка» и некоторые растворители способны оказать на него воздействие. Это свойство очень важно для организации процесса добычи.
- Более низкая температура плавления по сравнению с другими металлами и минералами, что позволяет выплавлять золото из изделий и изготавливать украшения из расплава.
Внимание. Находясь в расплавленном состоянии, золото быстро улетучивается, что надо учитывать при его плавлении.
Где содержится золото
Домашнему умельцу необходимо настраиваться на трудоемкий и кропотливый процесс, т.к. доступное сырье имеет мизерное золотое содержание, причем трудноизвлекаемое. Драгоценный металл можно добыть из таких материалов:
- Детали радиоаппаратуры и электронных устройств – микросхемы, транзисторы, диоды, конденсаторы, резисторы, переключатели, материнские платы, разъемы, процессоры. Достаточное для извлечения количество золота содержится в реле типа РЭС, РПС, РПВ, РКГ; лампах старых радиоприемников и телевизоров. Особо выделяются радиолампы серии ГМИ. Золотосодержащие детали можно найти в телевизорах, радиоприемниках, компьютерах, магнитофонах, видеомагнитофонах, мобильных телефонах, холодильниках и другой бытовой технике. Наличие таких деталей, как правило, указывалось в паспорте на аппаратуру. Современные технологии позволяют обойтись без использования драгметаллов, а потому их следует искать в деталях старых приборов и устройств. Надо отметить, что изделия советского производства отличались большим количеством ценных деталей.
- Бижутерия. Золото можно извлечь из испорченных, поврежденных, пришедших в негодность сережек, колец, подвесок, кулонов, брошей и других украшений, имеющих позолоту или вкрапление ценных элементов.
- Часы. Интерес представляют изделия с напылением на корпусе или стрелках, браслеты.
- Столовые приборы и сувениры. Это могут быть вилки, ложки, посуда, статуэтки, декорирующие элементы с золотым напылением.
Интересно: Покупаем слитки серебра в Сбербанке — нюансы и цены
Процесс добычи в домашних условиях по шагам
Золотодобыча в домашних условиях может быть организована несколькими способами. Они основываются на следующих принципах:
- Растворение основы. Изделия с поверхностной позолотой (часы, посуда) для получения драгметалла достаточно подвергнуть воздействию мощного растворителя. В основе этой методики лежит уникальная инертность золота, на которое не действует даже концентрированная кислота. Для реализации метода достаточно изделия с напылением поместить в стеклянную емкость и залить концентрированной азотной кислотой. Все металлические детали растворятся через 3-4 дня, а золото выпадет в осадок.
- Вытравливание. Этот принцип основывается на полном растворении деталей. Для того чтобы растворить золото потребуется «адская смесь» в виде сочетания соляной и азотной кислоты – «царская водка». В такой жидкости золото только растворяется, а все остальные ингредиенты не просто растворяются, а химически реагируют с кислотой, образуя соответствующие соединения. В этих условиях введение нужных реагентов позволяет осадить золото из раствора. В качестве их можно использовать гидрохинон, гидразин, перекись водорода, сульфит натрия, железный купорос. Технология вытравливания наиболее подходит для извлечения золота из мелких деталей электронных устройств.
- Электролиз. Золото высокой пробы можно получить путем электролиза. Золотосодержащая радиодеталь служит анодом, а в качестве катода устанавливаются 2 свинцовые или железные пластины, соединенные сверху проводником. Электролит – соляная кислота. При пропускании постоянного электрического тока (с плотностью 0,6-0,7 А/кв.дм площади анода) золото постепенно переходит на катодные пластины и оседает на их поверхности.
Методики вытравливания золота
При реализации указанных методик получения золота из различных деталей необходимо соблюдать определенный порядок действий. Первый вариант добычи предусматривает такие работы:
- Накопление достаточного количества сырья. Удаление всех элементов, не имеющих ценности. Для обработки подготавливаются только элементы с золотым напылением с минимальным содержанием других материалов.
- Помещение сырья в стеклянную емкость и заливка концентрированной азотной кислотой.
- Через 3-4 суток (при условии полного растворения основы) производится фильтрация раствора через марлевые слои.
- Полученный осадок помещается в стеклянную тару и заливается этиловым спиртом или водкой. Выдержка составляет 22-25 ч.
- Осадок коричневого оттенка промывается и фильтруется, после чего направляется на плавление. Для получения более чистого металла рекомендуется в расплав добавить соду.
Наиболее часто золото из радиодеталей добывается путем вытравливания. Эта технология реализуется в такой последовательности:
- Накопление достаточного количества сырья для переработки.
- Приготовление «царской водки». В стеклянной емкости смешивается соляная (3 части) и азотная (1 часть) кислота с соблюдением максимальной осторожности.
- Сырье очищается от грязи и загружается в «царскую водку».
- Производится нагрев жидкости для ускорения растворения. Процесс считается завершенным, когда детали полностью растворятся, а раствор приобретет ярко-зеленый цвет.
- Осаждение золота. Для этих целей можно использовать раствор гидрохинона, приготавливаемый путем добавления 50 г в 1 л воды. Этот состав аккуратно выливается в сосуд с «царской водкой», придерживаясь концентрации 10 мл гидрохинона на 1 л растворителя. Далее, емкость оставляется на 3,5-4 ч.
- Раствор аккуратно фильтруется, а затем осажденное на дно емкости золото выпаривается и высушивается. Осадок имеет вид тонких лоскутков фольги желтого цвета.
Домашняя золотодобыча характеризуется мизерными порциями драгоценного металла, а потому надо минимизировать его потери. Так, на окончательной стадии выпаривания золота рекомендуется в полученный осадок добавить буру и соду, что снизит отходы и упростит дальнейшую обработку. Получаемый металл лучше сразу заливать в специально приготовленные формы (тигели).
Для плавления золота используются небольшие горелки или муфельные печи. Формы изготавливаются из чугуна или легированной стали и имеют разборную конструкцию. Чаще всего, золото хранится в виде небольших слитков. В зависимости от количества полученного окончательного продукта, ему иногда придают форму прутков или проволоки.
Особенности работы с реагентами
При домашней добыче золота придется иметь дело с очень агрессивными и вредными химическими веществами. Необходимо помнить, что кислотные пары (особенно при нагревании) крайне опасны для человеческого организма.
В процессе работ выделяется оксид азота, способный поражать дыхательную систему, вплоть до летального исхода. Частое и продолжительное вдыхание вредных веществ может вызвать хронические заболевания. Концентрированные кислоты способны приводить к тяжелым химическим ожогам, как кожного покрова, так и слизистых оболочек.
Важно. При проведении работ в домашних условиях необходимо строго соблюдать меры предосторожности. На всех этапах должно обеспечиваться хорошее вентилирование помещения. Работать можно только в резиновых перчатках, защитных очках, респираторе и защитном фартуке.
Интересно: Сколько стоит грамм золота в ломбарде
Использование полученного золота
Золото, добытое в домашних условиях, можно использовать по-разному. При этом, не следует забывать, что получение постоянного дохода таким способом требует получения соответствующей лицензии. В целом, выделяются такие варианты:
- Продажа золота в слитках или сдача их на реализацию. Для придания нужного внешнего вида они подвергаются полировки с использованием зубной пасты, наносимой на шероховатую поверхность металла войлоком.
- Приготовление ювелирного припоя для ремонта золотых украшений. Такой припой изготавливаются путем смешения полученного золота с различными присадками. Например, для ремонта изделий с 585 пробой используется такой рецепт припоя: золото – 585 частей по массе (в.ч.), медь – 185 в.ч., серебро – 116 в.ч., кадмий – 112 в.ч. Для удобства использования припой готовится в форме пасты – тиноля.
Изготовление ювелирных украшений
В домашних условиях можно изготовить различные простые ювелирные украшения – сережки, кулоны, кольца, перстни, цепочки. Наиболее распространенный способ – литье в специальные формы. Полученный драгметалл расплавляется в небольших емкостях с носиком.
Нагрев до нужной температуры обеспечивает муфельная печь. Далее, расплав тонкой струйкой направляется через отверстие в форму. При необходимости производится аккуратная ковка металла.
Изготовление сложных изделий требует наличия набора специальных инструментов ювелира.
Добыча золота дома, своими руками – это, хотя и трудоемкий, но вполне выполнимый процесс. Драгоценный металл можно найти в старой радиоаппаратуре и различных электронных устройствах. Для извлечения его требуются химические реагенты, при работе с которыми необходимо соблюдать максимум осторожности. Золото лежит без дела рядом, и его можно добыть без поиска золотоносной жилы.
Источник: https://yainvestor.guru/idei-investitsij/dragmetally/hand-made-gold
Чем и как можно растворить золото?
Растворители золота встречаются нечасто, причина в том, что металл неспроста относят к благородным, он инертен и не вступает в реакции с химическими реагентами. По этой причине жидкостей и элементов, с которыми золото взаимодействует, не так много. Современные химики используют опыт поколений и по старинке растворяют металл в царской водке, которая впервые была описана алхимиком в XIV веке.
Что такое царская водка?
Растворение золота — процесс сложный и трудоемкий, по этой причине алхимики на протяжении нескольких веков пытались найти универсальный растворитель. Он был необходим им не только для опознания металла, но и для превращения железа в золото.
Растворение золота в царской водке
Первые описания царской водки появились еще задолго до того, как была открыта соляная кислота. Путем проб и ошибок Псевдо-Гебером была получена смесь, которая, по его мнению, могла растворить любой металл, в том числе и золото. Случилось это в Европе. Реакция проходила с использованием следующих компонентов:
- селитры;
- медного купороса;
- нашатыря;
- кварца.
Процесс получения растворителя проходил методом сухой перегонки. Алхимик рекомендовал готовить смесь в посуде из стекла, которая была плотно запаяна.
Вторичной водкой смесь азотной и соляной кислоты называл ученый Альберт Великий. Первичной водкой он считал азотную кислоту.
Бонавентура, третий исследователь, описал смесь кислот как растворитель, он изложил на бумаге свои опыты, а раствор, который смог получить, назвал «крепкой водкой».
Ученные из Царской России также питали интерес к химии, одним из первых, кто описал в своих работах смесь соляной и азотной кислот, стал Михаил Ломоносов.
Примечателен и тот факт, что изначально слово «водка» не имело никакой связи с крепкими спиртными напитками. Она происходила от слова вода, только в форме уменьшительно-ласкательной.
В воде золото не растворяется — это известно всем, но вот смесь кислот обладает прозрачностью, которая свойственна воде, по этой причине ее и назвали водкой.
Когда золото начинает растворяться или раствор взаимодействует с воздухом, то реакция проходит с выделением газа. Ранее считалось, что это пары драгоценного металла, которые испаряются во время реакции, но с годами стало известно, что газ, который выделяется в период растворения золота, — это хлор.
Свойства царской водки:
- растворяет золото и металлы платиновой группы при условии, что в реакции участвует кислород;
- используется в процессе аффинажа драгметаллов;
- смесь кислот прозрачная, но с течением времени раствор постепенно приобретает оранжевый оттенок и теряет свойства.
Золото растворяется в растворе при комнатной температуре, но если есть необходимость ускорить реакцию, то смесь кислот нагревают.
Можно отметить и еще несколько свойств царской водки:
- Не растворяет серебро (металл образует пленку).
- Не растворяет тефлон.
- Цирконий, хром, титан и другие элементы отличаются чувствительностью к раствору.
Описывая свойства царской водки, можно вспомнить один интересный факт, когда немецким ученым удалось сохранить свои награды.
Получение Нобелевской премии в Германии в период правления Адольфа Гитлера было запрещено. По причине того, что как-то раз награду получил немецкий химик и противник национал-социалистической партии Карл фон Осецкий.
Два физика из Германии, опасаясь конфискации, передали свои награды химику Дьёрдью де Хевеши. Он спрятал медали, но когда немцы оккупировали Копенгаген, химик испугался того, что награды будут изъяты. Он растворил медали в царской водке и поставил банку на полку. Обыскивая помещение, немецкие военные не обратили внимания на раствор.
После окончания войны химик восстановил золото и отправил его вместе с письмом Шведской королевской академии, произошло это спустя три года. Нобелевский фонд изготовил из золота новые медали и вернул их владельцам.
Какие растворители существуют еще?
Как растворить золото, не используя соляную и азотную кислоты? Для этого понадобится еще одна кислота, синильная. Такой метод растворения осуществим путем цианирования руд. В основном применяется в промышленности, потому что считается технологически сложным процессом, который нельзя осуществить в домашних условиях.
Каким образом проходит процесс:
- подготавливается площадка, которая не пропускает воду;
- на площадку помещается руда, в состав которой входит благородный металл;
- руду орошают растворами цианидов;
- цианиды просачиваются через породу и растворяют золото;
- металл в растворенном виде оседает в колоннах.
Долгое время цианирование проходило немного иначе, сегодня процесс технически доработан и носит иное название — крупное выщелачивание.
Используется для извлечения золота из пород руды на крупных предприятиях. Но процедура имеет несколько минусов из-за того, что получить золото таким образом можно не из всех руд. Необходимо учитывать свойства металла.
Если речь идет о сульфидных рудах, то для того, чтобы извлечь из них благородный металл, придется использовать сложные технологии. Необходимо подвергать породу специальным системам очистки, которые называют аффинажем и используют на заводах.
Растворяется золото и при контакте со ртутью, но это не совсем то, что необходимо. Амальгама — это сплав ртути и золота. Этот способ интересен тем, что для того чтобы получить благородный металл, породу смешивали со ртутью и дополнительно измельчали ее в мельницах. Ртуть образовывала сплав с золотом. Сплав разрушали при помощи промывки, после чего ртуть извлекали и использовали повторно, поскольку свойств своих она не теряла.
Примечательно, что этот метод известен человечеству еще с I века нашей эры, но масштабно его стали применять лишь в XVI веке, произошло это в Испании, территория которой на тот момент являлась колонией американцев. Причиной всему было крупное месторождение ртути. Позднее технологию усовершенствовали. Стали использовать шлюзы с пластинами из меди, на которые ртуть была нанесена тонким слоем.
Источник: https://HochuZoloto.com/svojstva/rastvoriteli-zolota.html
В чем растворяется золото: обзор химикатов, способных растворить золото
Золото — крайне малоактивный металл. Даже в природе оно встречается, в основном, в виде самородков (в отличие от щелочных и щелочноземельных металлов, находящихся исключительно в составе минералов или других соединений). При долгом нахождении на воздухе оно не окисляется кислородом ( сей благородный металл ценят в том числе и за это). Поэтому найти, в чем растворяется золото, достаточно сложно, но можно.
Промышленный метод
При добыче золота из так называемых золотоносных песков приходится работать со взвесью примерно одинаково мелких частиц золота и песчинок, которые нужно отделить друг от друга. Можно сделать это с помощью промывания, а можно использовать цианид натрия или калия — разницы нет. Дело в том, что золото образует растворимый комплекс с цианид-ионами, а песок не растворяется и остается как есть.
Ключевым моментом в этой реакции является наличие кислорода (того, что содержится в воздухе, достаточно): кислород окисляет золото в присутствии цианид-ионов и получается комплекс. При недостаточном количестве воздуха или сама по себе без цианида реакция не идет.
Сейчас это наиболее распространенный способ промышленного получения золота. Конечно, до получения конечного продукта еще много стадий, но нас интересует конкретно этот этап: растворы цианидов — то, в чем растворяется золото.
Процесс амальгамации также применяют в промышленности, только уже при работе с рудами и твердыми породами. Суть его заключается в способности ртути образовывать амальгаму — интерметаллическое соединение. Строго говоря, ртуть в этом процессе не растворяет золото: оно остается в амальгаме в твердом виде.
При амальгамации идет смачивание породы жидкой ртутью. Однако процесс «вытягивания» золота в амальгаму долгий, опасный (пары ртути ядовиты) и малоэффективный, поэтому этот метод уже редко где применяют.
Царская водка
Есть много кислот, способных разъедать живые ткани и оставлять страшные химические ожоги (вплоть до летального исхода). Однако нет такой одиночной кислоты, в какой растворяется золото.
Из всех кислот подействовать на него может только знаменитая смесь — царская водка. Это азотная и соляная (хлороводородная) кислоты, взятые в соотношении 3 к 1 по объему.
Замечательные свойства этого адского коктейля обусловлены тем, что кислоты берутся в очень больших концентрациях, что сильно повышает их окислительную способность.
Царская водка начинает действовать с того, что азотная кислота начинает окислять сперва соляную, и в ходе этой реакции образуется атомарный хлор — очень реакционноспособная частица. Именно она идет на атаку золота и образует с ним комплекс — золотохлористоводородную кислоту.
Это очень полезный реактив. Очень часто золото хранят в лаборатории именно в виде кристаллогидрата такой кислоты. Нам же оно служит лишь подтверждением того, что золото растворяется в царской водке.
Стоит еще раз обратить внимание на то, что окисляет металл в этой реакции не одна из двух кислот, а продукт их взаимной реакции. Так что если взять, например, одну лишь «азотку» — известную кислоту-окислитель — ничего не выйдет. Ни концентрация, ни температура не смогут сделать так, чтобы золото растворилось в азотной кислоте.
Хлорка
В отличие от кислот, в частности хлороводородной кислоты, отдельные вещества могут стать тем, в чем растворяется золото. Широко известная бытовая хлорка — раствор газообразного хлора в воде. Конечно, обычным магазинным раствором ничего не сделаешь, нужны концентрации повыше.
Хлорная вода действует следующим образом: хлор диссоциирует на соляную и на хлорноватистую кислоты. Хлорноватистая кислота под светом разлагается на кислород и соляную кислоту. В таком разложении выделяется атомарный кислород: как и атомарный хлор в реакции с царской водкой, он очень активен и окисляет золото за милую душу. В итоге опять получается комплекс золота с хлором, как и в предыдущем способе.
Другие галогены
Кроме хлора, золото также неплохо окисляют и другие элементы седьмой группы таблицы Менделеева. В полной мере сказать о них: «то, в чем растворяется золото» — трудно.
С фтором золото может реагировать по-разному: при прямом синтезе (с температурой 300-400°С) образуется фторид золота III, который в воде немедленно гидролизуется. Он настолько неустойчив, что разлагается даже при воздействии плавиковой (фтороводородной) кислоты, хотя среди фторид-ионов ему должно быть комфортно.
Также действием сильнейших окислителей: фторидов благородных газов (криптона, ксенона) можно получить и фторид золота V. Такой фторид вообще взрывается при контакте с водой.
С бромом дела обстоят несколько проще. Бром в обычных условиях — жидкость, и золото неплохо рассеивается в его растворах, образуя растворимый бромид золота III.
С йодом золото также реагирует при нагревании (до 400°С), образуя йодид золота I (такая степень окисления объясняется меньшей активностью йода по сравнению с другими галогенами).
Таким образом, золото, несомненно, реагирует с галогенами, однако растворяется ли золото в них — спорное утверждение.
Раствор Люголя
На самом деле, йод (обычный йод I2) в воде нерастворим. А растворим его комплекс с йодидом калия. Это соединение называется раствором Люголя — и он умеет растворять золото. Между прочим, им же часто смазывают горло болеющим ангиной, так что не все так однозначно.
Эта реакция также идет через образование комплексов. Золото образует с йодом комплексные анионы. Используется, как правило, для травления золота — процесс, при котором взаимодействие идет только с поверхностью металла. Раствор Люголя удобен в этом случае, потому что в отличие от царской водки и цианидов, реакция идет заметно медленнее (и реактивы доступнее).
Бонус
Говоря о том, что одиночные кислоты — это то, в чем золото не растворяется, мы немного соврали — на самом деле такие кислоты есть.
Хлорная кислота — одна из самых сильных кислот. Ее окислительные свойства чрезвычайно высоки. В разбавленном растворе они проявляются плохо, однако в больших концентрациях творят чудеса. При реакции образуется ее соль перхлорат золота — желтый и неустойчивый.
Из кислот, в каких растворяется золото, есть еще горячая концентрированная селеновая кислота. В результате также образуется соль — селенат золота красно-желтого цвета.
Источник: https://FB.ru/article/384182/v-chem-rastvoryaetsya-zoloto-obzor-himikatov-sposobnyih-rastvorit-zoloto
В чем растворяется золото: обзор химикатов, применение кислот, какой способ подходит для домашних условий
Добрый день, читатели! В этой статье вы найдете информацию об одном из самых сложных процессов в химии — растворении золота. С помощью моих советов вы сможете воссоздать тяжелейшую реакцию самостоятельно и без особых навыков!
Золото — довольно малоактивный металл. В природе чаще всего оно встречается в качестве соединений. Когда неопытный химик задается целью получить чистый драгметалл, сам собой возникает вопрос, в чем растворяется золото. Без растворения выделить его невозможно. Но найти вещество, которое вступит в сложную реакцию, — непростая задача, не зря ведь золото называют благородным металлом.
Чем можно растворить золото
Долгие годы химики использовали лишь опасный метод, в котором при предельно высокой температуре золото растворяется в реакции с фтором. Но в современном мире применяют новые, более безопасные способы.
Амальгама
Амальгамой называют сплавы ртути в жидком или твердом состоянии, его используют как промышленный метод аффинажа. Процесс амальгамации золота заключается в особенности ртути образовывать соединения нескольких металлов.
Перед амальгамацией следует поместить самородок в раствор азотной кислоты в соотношении с водой 10:1. Золото должно находиться в растворе до полного завершения видимой реакции, после чего его необходимо промыть.
Для амальгамации драгметалл и ртуть берутся в одинаковой пропорции. В неметаллический лоток помещают оба вещества и вращают его. Шарик ртути растворяется в молекулах самородка. Ненужный осадок выливается из лотка.
Насыщенную золотом амальгаму необходимо осторожно промыть под проточной водой.
Излишки ртути из амальгамы удаляются путем продавливания шарика через мокрую замшу. Оставшееся на поверхности соединение нагревается до полного испарения ртути.
Какой способ подходит для домашних условий
Аффинаж золота (получение чистого металла) можно произвести и дома. Самый безопасный метод растворения — с помощью электрического тока.
Пошаговая инструкция по растворению золота
Растворение металла — трудоемкий процесс. Действенный способ — использование цинка. Он применяется химиками для выделения чистейшего металла высокой пробы.
Существует множество видео, на которых наглядно показана бурная реакция с цинком.
Необходимые материалы и инструменты
Требуются следующие инструменты:
- емкость для нагрева;
- большой пинцет;
- плита;
- огнеупорная колба;
- колпак с щелью;
- аппарат для плавления металлов.
Источник: https://zhazhdazolota.ru/dobycha/v-chem-rastvoryaetsya-aurum
Реактивы и ход процесса растворения золота
Растворители золота — это вещества, которые способны воздействовать на драгметалл и трансформировать элемент на некоторое время. У многих может возникнуть вопрос, зачем растворять золото? Этот процесс предназначен в первую очередь для очистки драгметалла от примесей и эффективной переработки отходов.
Растворение золота в царской водке
Процесс растворения
Растворяя золото, можно с помощью последующих процессов добиться высшей пробы, то есть увеличить количество драгметалла металла в сплаве. Процесс происходит в три этапа:
- Растворение золота с примесями.
- Выпаривание.
- Осаждение драгметалла.
Именно для первой стадии нужны растворители. Но не каждое сильнодействующее вещество подойдет для таких целей. Золото — благородный металл, что означает инертность вещества по отношению ко многим реактивам. Но в то же время существуют кислоты или смеси, которые способны растворить золото.
Растворение — сложный процесс, но можно выполнить его и в домашних условиях. Например, перед очисткой лома или извлечением драгметалла из радиодеталей. Но перед тем как добавлять реактивы в изделия, стоит очистить лом от примесей. Например, с помощью магнита избавится от ферромагнетиков. Затем лом можно опустить в азотистую кислоту, чтоб избавиться сразу от части металлов.
Реактивы (вещества) для первого этапа очистки
Среди реактивов, которыми можно растворить золото, самым известным и применяемым является царская водка, или Aqua Regia. Вещество очень популярное, его изучают даже на уроках химии в школе. Как растворить золото в царской водке — вопрос, который волнует домашних экспериментаторов. По составу царская водка — это смесь концентрированных азотной и соляной кислот в соотношении 1:3 по объему и 1:2 по массе. Около 65-67% приходится на азотную кислоту по массе и 33-36% — соляной кислоты.
Царским прозвали реактив, поскольку он мог растворить «царя металлов», ну а водка изначально была жидким веществом. Намного позже значение этого слова стало ассоциироваться с алкогольным напитком. С точки зрения химии, в результате реакции получается вещество — золотохлористоводородная кислота, или тетрахлораурат водовода.
Формула процесса выглядит так: Au + HNO3 + 4 HCl = HAuCl4 + NO + 2 H2O. Поэтому, ориентируясь на уравнение, для растворения 1 грамма золота необходимо 5 миллилитров царской водки. В реакции именно соляная кислота является растворителем, а азотная выступает в роли катализатора, то есть ускоряет процесс и компенсирует реакцию.
Поэтому в процессе растворения лучше всего брать 3,75 миллилитра соляной кислоты на грамм лома золота. После того как начнет происходить видимая реакция, выдержите металл в растворе до 5 минут и слейте кислоту, после чего залейте новой порцией вещества. Далее поставьте емкость с ломом и кислотой на плиту и нагревайте смесь, вливая в нее азотную кислоту в пропорции 1,25 миллилитр на 1 грамм металла.
Все реактивы должны быть просчитаны, особенно азотная кислота. Именно от этого вещества придется избавляться в процессе фильтрации и осаждения. После растворения металла не стоит добавлять азотную кислоту в раствор. После завершения процесса растворения необходимо продержать получившуюся смесь нагретой около 30 минут.
Следующим этапом будет фильтрация золота, которая происходит уже с помощью других веществ. Фильтрация — процесс, проходящий в два этапа. Перед фильтрацией после растворения нужно выдержать раствор около суток, поскольку за это время кислоты в составе царской водки испаряются. Само по себе вещество нестойкое, что облегчает последующую очистку драгметалла.
Осаждение золота
Из всех существующих веществ не только водка справляется с процессами растворения благородного металла. На золото действуют:
- Озон. В результате чего образуется оксид Аu2О3 коричневого цвета. В обычных условиях реакция невозможна, нужно большое количество концентрированного озона.
- Газообразный фтор, бром, йод, хлор также растворяют золото в нагретом состоянии. В результате процесса образуются фторид АuF3, красный хлорид АиС13, коричневый бромид АuВr3 и темно-зеленый йодид АuI3. Поэтому если у вас есть позолоченное украшение, лучше избегать контактов с йодной настойкой. Драгметалл способен растворяться в жидком броме, а с хлорной водой он реагирует при комнатной температуре, образовывая НАuСl4.
- А еще растворяется золото в концентрированной горячей селеновой кислоте. В процессе реакции кислота восстанавливается до селенистой. Химики записывают методику так: 2Аu + 6Н2SеO4 = Аu2(SеO4)3 + 3Н2Sе03 + 3Н20.
- Чтоб растворить драгметалл, нужно к горячей серной кислоте добавить окислитель. В роли окислителя используют нитрат, перманганат, хромовую кислоту, диоксид марганца.
- Можно провести процесс и с помощью цианидов щелочных и щелочноземельных металлов. Реакция происходит даже при нормальной температуре с доступом кислорода. Но в результате соединения золота с цианидом получаются очень прочными, поэтому в промышленных целях способ используют для очистки добытого золота от руд. 4Аu + 8КСN + 2Н2O + O2=4К[Аu(СN)2] + 4КОН — вот так выглядит реакция. Она была открыта и исследована русским ученым-инженером Багратионом. Процесс назвали цианированием.
- Существует и анодное растворение золота в щелочи КОН, при котором драгметалл образует аурат калия и анодный осадок.
Благородность золота, с точки зрения современной химии, все же не так совершенна, как хотелось бы. Конечно, в домашних условиях эти реакции проводить опасно, но в лабораториях и на заводах есть возможность за ними наблюдать. Эти реакции и позволяют экономнее относиться к сырью в виде золота, а также делать драгметалл более чистым. Перед проведением реакций убедитесь, что все реактивы подготовлены правильно и соблюдены меры предосторожности.
А чтоб уберечь свое изделие из золота от негативных реакций, лучше не контактируйте с йодной настойкой. Особенно от воздействия веществ следует беречь украшения с меньшим составом драгметалла, поскольку лигатура быстрее реагирует на химические реактивы.
Рекомендуем другие статьи
Источник: https://DedPodaril.com/zoloto/imform/rastvoriteli-zolota.html
Золото из радиодеталей: извлечение ценных материалов из микросхем и элементов электротехники
Многие, имея в своем распоряжении много радиодеталей, предпринимают попытки извлечь из них золото. Ведь давно известно, что золото лучше всего проводит электричество, поэтому его в незначительных количествах используют для изготовления различных радиодеталей. Особенно это касается микросхем, в них доля золота больше.
В интернете встречаются разные фото добычи золота из радиодеталей, на котором запечатлен процесс, и его результаты. Способов известно несколько, но рассмотрим те, которые подходят для домашнего применения.
Как определить золото
Отделить золото от других металлов в радиоэлементах не так просто, это долгий и опасный процесс. Металл проходит стадию рафинирования, отделяется от примесей. Аффинаж золота из радиодеталей в домашних условиях возможен, если соблюдать все правила безопасности.
Тому, кто в первый раз решился добыть золото, стоит знать, что после растворения всех элементов в кислоте о наличии там драгоценного металла можно только догадываться. Визуально его не заметить, результат будет виден только после завершения всех процедур.
Из каких деталей лучше извлекать золото
и количество золота в радиодеталях разное, оно встречается в деталях советского производства. В современных радиоэлементах встречается редко, особенно это касается заграничных изделий.
Как извлечь золотое напыление
Стоит отметить, что детали с желтым окрасом не всегда содержат золото. Многие хотят знать, в каких радиодеталях есть золото?
Чаще оно встречается в различных микросхемах, а так же транзисторах, диодах, стеклянных электродах, реле тоже имеют его напыление.
Перед добычей благородного металла нужно приготовить правильные пропорции реактивов. Далее все золотосодержащие элементы нужно промыть, не оставляя следов грязи.
Проделывать процедуру извлечения придется с опасными кислотами, которые представляют реальную угрозу жизни для человека. Поэтому инструкция, по извлечению золота из радиодеталей начинается с правила безопасности.
Какой химический реактив использовать
Добывать золото дома можно при помощи царской водки. Кто впервые слышит это название, может подумать, что это спиртной напиток, но спирт не способен растворять металлы.
Царская водка состоит из соляной и азотной кислот. Для ее получения нужно в определенной пропорции смешать два реагента. Если взять литр концентрированного азотного реагента, и добавить в него до 300 мл соляной кислоты, то получится царская водка.
Добычу золота с помощью кислот необходимо проводить в стеклянной таре. Приготовление нужного раствора следует осуществлять в холодной среде, это значит, что посуда, где смешиваются реагенты, должна располагаться в ледяной воде. В этой процедуре требуется крайняя осторожность и неспешность. Далее раствор следует медленно перемешать.
Растворять металлы в полученной смеси можно подогрев ее до 60-70 гр. Затем можно помещать радиоэлементы в жидкость, но делать это нужно не спеша, лучше не взбалтывать. Чтобы раствор дольше оставался чистым, не стоит в него погружать посторонние предметы или грязные детали.
Какие опасности и результаты
Чтобы извлечь золото из радиодеталей своими руками нужно ждать 6 часов, пока химические процессы не растворят все элементы. В это время бурно выделяется оксид азота, это токсичный дым желтого цвета, который представляет серьезную опасность для человека.
Один вдох этого газа способен привести к потере сознания. При плохой вентиляции возможен летальный исход!
После растворения элементов нужно приступать к следующим процедурам.
Золотого осадка в жидкости не будет видно, металлы в ней растворятся до состояния молекул.
Чтобы собрать драгметалл в единое целое воспользуемся гидразином. Он встречается в виде порошка и жидкости. Для завершения процедуры его нужно 250-300 гр, он добавляется в емкость с царской водкой. В результате должен образоваться коричневый осадок. Внешне похож он на ржавчину, если отсутствует, золота в деталях не использовалось.
Раствор процеживают, а хлопья очищают в царской водке, пока золото не приобретет свой должный вид.
Заключение
На самом деле способов аффинажа золота из деталей встречается несколько. Использование поваренной соли избавляет раствор от азотной кислоты. Так же гидрохинон уменьшает потери драгметалла во время его добычи.
Фото золота из радиодеталей
Также рекомендуем просмотреть: Помогите проекту, поделитесь в соцсетях 
Источник: http://sdelatlegko.ru/zoloto-iz-radiodetalej/