Как правильно соединить медный и алюминиевый провод
В старых зданиях часто можно встретить алюминиевую электрическую проводку. Теперь уже всем понятно, что это не лучший металл для тока. Сегодня при капитальном ремонте обычно меняют всю проводку старого здания. Однако при частичном ремонте возникает необходимость соединения алюминиевого и медного проводов.
Можно ли соединять алюминиевые провода с медными
Прежде всего нужно вернуться к школьной программе по химии и физике. Есть такое понятие как «гальванический элемент» – простая батарейка, генерирующая электрический ток. Он образуется путем взаимодействия металлов в электролите. Скручивание медной и алюминиевой проводки кабеля, по сути, будет той же самой батарейкой.
Соединения проводов
Гальванический ток быстро разрушает металл. Несмотря на то, что он не образуются в сухом воздухе, а скрутка в розетке не развалится за день, проблемы при долгой эксплуатации проводки обеспечены.
Спустя несколько месяцев или лет провода начнут разрушаться – это приведёт к росту сопротивления. Когда к розетке подключат мощный потребитель тока, скрутка перегреется. При регулярной эксплуатации такого соединения имеется риск возгорания.
Возгорания проводки
Правила запрещают скручивать алюминиевые и медные проводники напрямую. Однако в экстренных ситуациях переход необходимо сделать, потому нужно следовать определенным правилам.
Что будет при контакте меди и алюминия
Любой металл, в том числе медь и алюминий, окисляются под воздействием кислорода. Это приводит к образованию оксидной пленки на поверхности материала. В случае с медью она не препятствует прохождению электрического тока, но пленка на алюминии повышает его сопротивление.
В случае соединения проводов разнородные металлы начнут плотное взаимодействие. Алюминий считается более активным, потому при скоплении влаги на стыках (она в любом случае присутствует в воздухе) начинается процесс электролиза, то есть ионы алюминия постепенно переносятся на медь.
Скрутка металлов
В итоге один из проводников теряет свою массу. В алюминии образуются пустоты и пробои – они также окисляются, что ускоряет процесс электролиза. Скорость процесса зависит еще и от объема влаги. Ближе к концу реакции получается практически разрушенный алюминиевый проводник – его сечение уменьшается, а плотность тока возрастает. Как уже было описано выше, металл греется и возникает риск возгорания.
Правила соединения медных проводов с алюминиевым
Существуют безопасные способы соединения медных и алюминиевых проводов:
Болтовое соединение
Этот способ считается самым доступным, надежным и простым. Для обустройства понадобится:
- Болт;
- Гайка;
- Стальные шайбы (несколько штук);
- Гаечный ключ.
Вряд ли получится применить этот способ для соединения проводов в квартирной распределительной коробке – сегодня их делают слишком маленькими, а готовый соединительный узел выходит достаточно большим.
Однако, если в строении установлена коробка советских времен или приходится работать в распределительном щитке, то болтовой метод – наилучшее решение.
Его принято считать идеальным решением, если приходится коммутировать полностью несовместимые жилы – с разным сечением, из разных материалов, много/одножильные.
Важно! Болтовой метод позволяет соединить больше 2 проводников (их число зависит от длины болта).
Процесс устройства соединения:
- Каждый из проводов придется зачистить от слоя изоляции – на 2–3 см от края.
- Из очищенных концов собирается кольцо по окружности болта, чтобы они без проблем могли на него надеваться.
- Далее берётся болт, а на него надевается шайба, после чего кольцо медного провода, затем вторая шайба, кольцо алюминиевого проводника, в конце – третья шайба вся полученная конструкция затягивается гайкой.
- В конце необходимо обезопасить соединение, использовав изоляционную ленту. Важно не забывать, чтобы между алюминием и медью находилась промежуточная шайба. Если планируется работать с несколькими разными проводниками, то между жилами одинакового материала шайба не обязательна.
Болтовое соединение
Особым преимуществом этого метода считается универсальность соединения. Его можно раскрутить и заново скрутить в любой момент и, если понадобится добавить провода, либо изменить схему подключения.
Клеммы
Другой дешевый и простой способ соединения – клеммные колодки. Их легко найти и купить, особенно, если учитывать, что часто продаются не целыми секциями, а отрезается в необходимом для работы количестве. Колодки бывают разных размеров, что напрямую зависит от сечения проводников.
Клеммы
Клеммники для соединения алюминиевых и медных проводов представляют собой пластмассовый каркас на несколько ячеек. Внутри каждой находится латунная трубчатая гильза. С разных сторон внутрь клеммы продеваются зачищенные кончики проводов и зажимаются винтами. Обустройство соединения:
- Ослабить зажим, освобождая одну часть гильзы, чтобы продеть в гильзу оголённую часть провода.
- На конце проводника зачистить изоляцию – на 5–6 мм. Провод вставляется в колодку, винт зажимается, фиксируя металл на гильзе. Крепление должно быть закручено прочно, но не сильно, иначе оно перебьет жилу.
- Аналогичные действия для подключения медного провода – только с противоположной стороны клеммы.
Важно! Все этапы работы необходимо проводить последовательно, несмотря на то, что физически можно разжать оба винта, продеть провода и закрутить за раз. Это необходимо, чтобы медь и алюминий не соприкасались концами внутри гильзы.
Основным преимуществом клемм считается простота их устройства и скорость установки. Метод называют разъёмным – один из проводников можно без особых проблем вытащить, чтобы соединить другой.
Клеммы с рычагами
Колодки плохо подходят для работы с многожильными проводами. В таком случае сначала придется монтировать втулочный наконечник, который обжимается пучком жил.
Другая особенность клемм – под давлением винта при комнатной температуре алюминий иногда подтекает. Это приводит к необходимости регулярно проверять колодки и подтягивать контакты. Если этого не делать, контакт слабеет, соединение нагревается и искрит – появляется риск пожара.
Клеммные колодки Wago
Быстрый и простой способ соединения – жилы нужно предварительно зачистить и продеть в клеммы до упора. Там они автоматически фиксируются при помощи прижимной пластины – она сильно придавливает материал к шине. Прозрачный корпус клемм позволяет контролировать проход проводника. Проблема способа – одноразовость таких приспособлений.
Если нужен многоразовый зажим, то лучше купить рычажковые клеммы. Рычаг приподнимается, чтобы освободить проход в отверстие – туда вставляется зачищенный провод. Затем рычаг опускается, чтобы зафиксировать жилу внутри клеммы. Это разъемное соединение меди и алюминия – при необходимости рычаг поднимается, чтобы достать проводник наружу.
Интересно! Большой популярностью и доверием на рынке пользуются самозажимные приспособления «WAGO». Компания выпускает специальную серию клемм, оснащённых контактной пастой «Alu-plus». Это смесь, защищающая контакты алюминия и меди от образования коррозии. Модель можно отличить по специальной маркировке «Al Cu».
Пользоваться самозажимными конструкциями очень просто. На самой клемме указано, на какую длину требуется зачистить изоляцию жилы.
Заклепки
Заклепки используются для обустройства неразъемного соединения, которое обладает теми же преимуществами, что и резьбовое, но не предполагает разборку и повторную сборку без разрушения заклепки и требует специального инструмента – соединителя.
Сегодня метод чаще используют для соединения тонкостенных элементов при формировании перегородок и интерьера разных помещений. Электрики выбирают заклепки из-за их низкой стоимости, прочности и простоты монтажа.
Заклепки
Принцип монтажа электросоединения прост: происходит втягивание и обрезание металлического стержня, продетого через трубчатую заклепку со шляпкой. У стержня предусмотрено утолщение – он расширяет заклепку, когда проходит через трубку. Фиксаторы бывают разной длины и размера.
Перед соединением проводов их нужно подготовить таким же способом, как и в случае с резьбовой связкой. Диаметры колечек должны быть слегка больше диаметров заклепок – оптимальный равен 4 мм. На заклепку сперва надевают алюминиевую жилу, потом пружинную шайбу, дальше медный проводник и вторую шайбу. Стальной стержень продевается в электроустановку и инструмент зажимает до щелчка (так обрезаются стальные излишки). Все готово.
Соединения, как резьбовые, так и неразъемные характеризуются надежностью. Этот методы используется для сращивания, к примеру, поврежденной при ремонтных работах алюминиевой проводки. Обязательно нужно обустроить изоляцию оголенных участков.
Паяльник
Пайка проводов, состоящих из разных металлов – вполне реализуемое решение, если учитывать определенные правила работы. Медь не вызывает трудностей при спаивании, чего не скажешь об алюминии. На его поверхности образуется амальгама, которая характеризуется сильной химической стойкостью – она не обеспечивает припою должной адгезии.
Спаянные провода
Для работы с двумя разнородными металлами проводов придется подготовить раствор медного купороса, батарейку типа «Крона» и отрезок медной проволоки. На алюминиевой жиле аккуратно зачищается будущее место пайки. Потом на это место наносится раствор медного купороса.
Медную проводку соединяют с положительным полюсом батареи «Крона» и погружают в раствор купороса. К отрицательному полюсу подключается алюминиевый проводник. Через некоторое время на алюминии отложится медный слой – на него припой цепляется без проблем.
Переходники для соединения с алюминия на медь
Гильзовые переходники для опрессовки считаются самым надежным и качественным соединением. Изготавливаются специальные медно-алюминиевые модели, в которые заводятся 2 провода, после чего они обрабатываются прессом. Однако нужно отметить, что гильзы предполагают сечения начиная с 16 мм2, тогда как в жилых зданиях используется от 1,5 до 4 мм2. Потому подключение лучше вести с использованием стандартной алюминиевой гильзы. Опрессовка происходит по алгоритму:
- Зачистить концы медного проводника лудим свинцово-оловянным припоем – это помогает предотвратить контакт металлов.
- Избавиться от оксидной пленки алюминия.
- Продеть провода с разных концов и опрессовать.
- Обмотать соединения изолентой или термоусадкой с последующим нагревом.
Важно! При чрезмерном обжиме внутри конструкции спаянный слой на медном конце может повредиться, потому размер гильзы и матрицы должен подходить под жилу.
Переходник с алюминия на медь хорош тем, что его можно заделывать под штукатурку, не опасаясь возгорания проводки. Однако, для реализации потребуется пресс, который влечёт за собой определённые затраты.
Гильзы
Рекомендуется, чтобы при производстве работ вся электропроводка была цельной, без обрывов и соединений – так снижается риск возгорания. Однако, если возникает острая необходимость, состыковать медную и алюминиевую жилу, то нужно учитывать все рекомендации и выбрать один из наиболее оптимальных методов.
Источник: https://rusenergetics.ru/provoda-i-kabeli/kak-soedinit-medniy-i-alyuminieviy
Как правильно выбрать велосипед для города?
Велосипед является весьма распространенным и удобным транспортным средством, которое набирает все больше популярности в крупных городах.
Причина этому проста, за счет своей маневренности и удобства человек легко может добраться из точки А в точку Б минуя пробки и давки в общественном транспорте.
А если прибавить к этому огромную пользу для экологии и собственного здоровья, то данный транспорт становится и вовсе одним из лучших. Но, чтобы езда на велосипеде была удобной и доставляла удовольствие его нужно правильно выбрать. Об этом мы и поговорим сегодня.
Одно из важнейших преимуществ городских велосипедов является отсутствие необходимости их регулярно обслуживать. Отчасти это связано с тем, что их ключевые детали и механизмы надежно спрятаны и защищены. При этом, такие модели зачастую имеют фары, поворотники и сигналы, что также очень удобно для езды среди автомобилей.
Данная категория велосипедов имеет также и высокую посадку, что позволяет сидеть как на стуле и создает удобный угол обзора. Подобные модели оказывают достаточно высокую нагрузку на позвоночник за счет своей конструкции, в связи с чем, седло имеет специальные пружины внизу, что повышает удобство при езде.
Велосипедная рама
Рамы у подобных велосипедов могут быть трапециевидными и без верхней трубы. На моделях с открытой трубой гораздо легче садиться, что весьма актуально если на вас длинное пальто или юбка (поэтому их еще называют женскими). Вам не нужно высоко задирать ногу при посадке садясь на такой велосипед.
В то же время чтобы открытая рама хорошо переносила нагрузки ее делают более жесткой из-за чего вес велосипеда становится больше. В связи с этим если при выборе средства передвижения для вас ключевой критерий легкость и манёвренность, то лучше покупать модель с трапециевидной рамой.
Стоит учитывать, что при выборе закрытого велосипеда дистанция между телом и трубой не должна быть меньше 10 см, чтобы снизить риск серьезной травмы при жестком соскальзывании.
Материал
Прочность и легкость велосипеда зависит как от типа конструкции рамы, так и от материала, из которого она сделана. На сегодняшний день распространены данные материалы:
Алюминий. Один из самых популярных материалов для велосипедов с лучшим соотношением критериев цена/качество. При этом, алюминий достаточно легкий, прочный и не подвержен воздействию коррозии.
Сталь. Еще один весьма распространенный материал, который отличается высокой прочностью и долгим сроком службы. В велосипедах используется хромированная сталь, обеспечивающая большую долговечность и красивый внешний вид.
Карбон. Велосипеды из данного материала отличается очень небольшим весом, но и высокой ценой. Также, карбон не отличается высокой прочностью, поэтому велосипеды из данного материала не подойдут для высоких нагрузок.
Амортизация
В городских моделях велосипедов есть два вида амортизации — ригид и хардтейл.
Если вы покупаете велосипед с целью езды по ровным асфальтированным дорогам и не готовы к большим затратам, то лучшим вариантом будет покупка велосипеда без амортизации или с амортизацией ригид.
В случае, когда дороги в вашем городе не всегда ровные и гладкие, или вы предпочитаете часто выезжать на природу, то лучше воспользоваться системой хардтейл, где имеется амортизационная вилка. Подобные модели весят немного больше, а сама амортизационная вилка требует определенного ухода, но зато даже самые неровные дороги не вызовут у вас никакого дискомфорта.
Ряд моделей оснащены специальной системой (LockOut), которая полностью блокирует работу вилки. Она может хорошо помочь, когда вы въезжаете в горку и 100% усилий от работы ног передастся заднему колесу велосипеда.
Седло
Когда время вашей езды не превышает одного часа, а ездите вы в спокойном темпе и не планируете совершать длительные поездки, то лучшим вариантом будет мягкое широкое седло, а также гелевые аналоги. Данные модели обеспечат вам наиболее комфортную езду.
Если же вы любитель длинных поездок на велосипеде, то вам следует присмотреться к жесткому седлу. В данном случае вашей точкой опоры будут седалищные кости, а ткани и сосуды не будут пережиматься. В случае, когда для долгих поездок используется мягкое седло, есть риск возникновения натертостей и пережатых сосудов.
Колёса
Диаметр у колес городского велосипеда может варьироваться от 26″ до 28″. Модели с диаметром 28″ гораздо легче преодолевают разного рода препятствия за счет более оптимального угла. На моделях с подобными колесами гораздо легче заехать на маленькое возвышение, вроде бордюра.
Однако, модели имеющие колеса 26″ являются более маневренными и легкими. Но разница между моделями с разными колесами совсем небольшая и практически не ощущается при езде.
Переключение скоростей
Когда в городе совсем незначительный перепад высот, то прекрасно подходит односкоростной велосипед. Подобные модели легкие и довольно доступные в плане цены. Однако для езды по неровным поверхностям больше подойдут велосипеды с переключением скоростей.
Если вы заинтересованы в модели, где механизм переключения передач наиболее надежный, то вам стоит присмотреться к велосипедам с встроенной планетарной втулкой. В данных моделях корпус втулки защищает все важные детали, что благоприятно влияет на надежность и долговечность велосипеда.
Тормоза
Есть велосипеды с барабанными тормозами, располагающиеся сзади модели в специальной втулке и помогающие тормозить, когда педали вращаются назад. Но подобная тормозная система не всегда удобна, так как требует перехода от езды к торможению, а если цепь слетит, то будет вовсе бесполезна.
Однако, преимущественно в городских велосипедах используются ободные тормоза. Вам нужно лишь нажать на специальный рычаг, которые расположен на руле, и тормозные колодки зажмут колесо велосипеда. Подобная тормозная система более надежна и при необходимости легко ремонтируется.
Лучше приобрести модель с ободными тормозами. Подобная конструкция обеспечивает лучшее торможение на скользкой или мокрой дороге, и является более безопасной.
Дополнительные комплектующие
Для велосипеда имеется множество дополнительных комплектующих, которые могут быть очень полезны. Стоимость всего комплекта может доходить до одной трети цены на велосипед. Как правило, стандартный набор представляет следующее:
- Отвертка с несколькими шестигранниками;
- Насос;
- Заднее зеркало;
- Защитный замок от угона;
- Велосипедные очки;
- Дополнительная камера;
- Специальная смазка для велосипедной цепи;
- Защитный шлем;
- Перчатки (это не обязательно, но с ними езда гораздо удобнее).
Цены
- От 120 до 250 долларов. Это преимущество китайские модели. Подобные велосипеды не отличаются высокой безопасностью и быстро ломаются.
- От 250 до 400 долларов. Весьма бюджетные модели, которые прекрасно подойдут если вы мало катаетесь (до 2 часов в день).
- От 450 до 750 долларов. Весьма неплохие велосипеды, которые подходят для тех, кто регулярно ездит по городу и привык к поездкам как к ровным дорогам, так и по сельской местности.
- От 1 000 до 2 000 долларов. Самая дорогая категория велосипедов. Используются для езды по любой местности, имеют долгий срок службы и почти не требуют дополнительного обслуживания.
Источник: https://cross.expert/sportivnaya-ekipirovka/velosiped-dlya-goroda.html
Свойства алюминия и области применения в промышленности и быту (стр. 1 из 4)
Федеральное агентство по образованию РФ
Государственный технологический университет
«Московский институт стали и сплавов»
Российская олимпиада школьников
«Инновационные технологии и материаловедение»
II-й этап: Научно-творческий конкурс
Направление (профиль):
«Материаловедение и технологии новых материалов»
РЕФЕРАТ
на тему:
«Свойства алюминия и области применения в промышленности и быту«
Работу выполнил:
Зайцев Виктор Владиславович
Москва, 2009
1. Введение
1.1 Общее определение алюминия
1.2 История получения алюминия
2. Классификация алюминия по степени чистоты и его механические свойства
3. Основные легирующие элементы в алюминиевых сплавах и их функции
4. Применение алюминия и его сплавов в промышленности и быту
4.1 Авиация
4.2 Судостроение
4.3 Железнодорожный транспорт
4.4 Автомобильный транспорт
4.5 Строительство
4.6 Нефтяная и химическая промышленность
4.7 Алюминевая посуда
5. Заключение
5.1. Алюминий — материал будущего
6. Список используемой литературы
1. Введение
В своём реферате на тему ”Свойства алюминия и области применения в промышленности и быту” я хотел бы указать на особенность этого металла и его превосходство перед другими. Весь мой текст является доказательством того, что алюминий метал будущего и без него будет трудным наше дальнейшее развитие.
1.1 Общее определение алюминия
Алюминий (лат. Aluminium, от alumen — квасцы) — химический элемент III гр. периодической системы, атомный номер 13, атомная масса 26,98154. Серебристо-белый металл, легкий, пластичный, с высокой электропроводностью, tпл = 660 °С. Химически активен (на воздухе покрывается защитной оксидной пленкой).
По распространенности в природе занимает 3-е место среди элементов и 1-е среди металлов (8,8% от массы земной коры). По электропроводности алюминий — на 4-м месте, уступая лишь серебру (оно на первом месте), меди и золоту, что при дешевизне алюминия имеет огромное практическое значение.
Алюминия вдвое больше, чем железа, и в 350 раз больше, чем меди, цинка, хрома, олова и свинца вместе взятых. Его плотность равна всего 2,7*103кг/м3. Алюминий имеет решётку гранецентрированного куба, устойчив при температурах от — 269 °С до точки плавления (660 °С). Теплопроводность составляет при 24°С 2,37 Вт×см-1×К-1.
Электросопротивление алюминия высокой чистоты (99,99%) при 20°С составляет 2,6548×10-8 Ом×м, или 65% электросопротивления международного эталона из отожжённой меди. Отражательная способность полированной поверхности составляет более 90%.
1.2 История получения алюминия
Документально зафиксированное открытие алюминия произошло в 1825. Впервые этот металл получил датский физик Ганс Христиан Эрстед, когда выделил его при действии амальгамы калия на безводный хлорид алюминия (полученный при пропускании хлора через раскаленную смесь оксида алюминия с углем). Отогнав ртуть, Эрстед получил алюминий, правда, загрязненный примесями. В 1827 немецкий химик Фридрих Вёлер получил алюминий в виде порошка восстановлением гексафторалюмината калием.
Современный способ получения алюминия был открыт в 1886 молодым американским исследователем Чарльзом Мартином Холлом. (С 1855 до 1890 было получено лишь 200 тонн алюминия, а за следующее десятилетие по методу Холла во всем мире получили уже 28000т. этого металла) Алюминий чистотой свыше 99,99% впервые был получен электролизом в 1920г. В 1925 г. в работе Эдвардса опубликованы некоторые сведения о физических и механических свойствах такого алюминия. В 1938г.
Тэйлор, Уиллей, Смит и Эдвардс опубликовали статью, в которой приведены некоторые свойства алюминия чистотой 99,996%, полученного во Франции также электролизом. Первое издание монографии о свойствах алюминия вышло в свет в 1967г. Еще недавно считалось, что алюминий как весьма активный металл не может встречаться в природе в свободном состоянии, однако в 1978г.
в породах Сибирской платформы был обнаружен самородный алюминий — в виде нитевидных кристаллов длиной всего 0,5 мм (при толщине нитей несколько микрометров). В лунном грунте, доставленном на Землю из районов морей Кризисов и Изобилия, также удалось обнаружить самородный алюминий. Предполагают, что металлический алюминий может образоваться конденсацией из газа.
При сильном повышении температуры галогениды алюминия разлагаются, переходя в состояние с низшей валентностью металла, например, AlCl. Когда при понижении температуры и отсутствии кислорода такое соединение конденсируется, в твердой фазе происходит реакция диспропорционирования: часть атомов алюминия окисляется и переходит в привычное трехвалентное состояние, а часть — восстанавливается. Восстановиться же одновалентный алюминий может только до металла: 3AlCl > 2Al + AlCl3.
В пользу этого предположения говорит и нитевидная форма кристаллов самородного алюминия. Обычно кристаллы такого строения образуются вследствие быстрого роста из газовой фазы. Вероятно, микроскопические самородки алюминия в лунном грунте образовались аналогичным способом.
2. Классификация алюминия по степени чистоты и его механические свойства
В последующие годы благодаря сравнительной простоте получения и привлекательным свойствам опубликовано много работ о свойствах алюминия. Чистый алюминий нашёл широкое применение в основном в электронике — от электролитических конденсаторов до вершины электронной инженерии — микропроцессоров; в криоэлектронике, криомагнетике.
Более новыми способами получения чистого алюминия являются метод зонной очистки, кристаллизация из амальгам (сплавов алюминия со ртутью) и выделение из щёлочных растворов. Степень чистоты алюминия контролируется величиной электросопротивления при низких температурах.
В настоящее время используется следующая классификация алюминия по степени чистоты:
Механические свойства алюминия при комнатной температуре:
Чистый алюминий — довольно мягкий металл — почти втрое мягче меди, поэтому даже сравнительно толстые алюминиевые пластинки и стержни легко согнуть, но когда алюминий образует сплавы (их известно огромное множество), его твердость может возрасти в десятки раз. Наиболее широко применяются:
Бериллий добавляется для уменьшения окисления при повышенных температурах. Небольшие добавки бериллия (0,01 — 0,05%) применяют в алюминиевых литейных сплавах для улучшения текучести в производстве деталей двигателей внутреннего сгорания (поршней и головок цилиндров).
Бор вводят для повышения электропроводимости и как рафинирующую добавку. Бор вводится в алюминиевые сплавы, используемые в атомной энергетике (кроме деталей реакторов), т.к он поглощает нейтроны, препятствуя распространению радиации. Бор вводится в среднем в количестве 0,095 — 0,1%.
Висмут. Металлы с низкой температурой плавления, такие как висмут, свинец, олово, кадмий вводят в алюминиевые сплавы для улучшения обрабатываемости резанием. Эти элементы образуют мягкие легкоплавкие фазы, которые способствуют ломкости стружки и смазыванию резца.
Галлий добавляется в количестве 0,01 — 0,1% в сплавы, из которых далее изготавливаются расходуемые аноды.
Железо. В малых количествах (»0,04%) вводится при производстве проводов для увеличения прочности и улучшает характеристики ползучести. Так же железо уменьшает прилипание к стенкам форм при литье в кокиль.
Индий. Добавка 0,05 — 0,2% упрочняют сплавы алюминия при старении, особенно при низком содержании меди. Индиевые добавки используются в алюминиево-кадмиевых подшипниковых сплавах.
Примерно 0,3% кадмия вводят для повышения прочности и улучшения коррозионных свойств сплавов.
Кальций придаёт пластичность. При содержании кальция 5% сплав обладает эффектом сверхпластичности.
Кремний является наиболее используемой добавкой в литейных сплавах. В количестве 0,5 — 4% уменьшает склонность к трещинообразованию. Сочетание кремния с магнием делают возможным термоуплотнение сплава.
Магний. Добавка магния значительно повышает прочность без снижения пластичности, повышает свариваемость и увеличивает коррозионную стойкость сплава.
Медь упрочняет сплавы, максимальное упрочнение достигается при содержании меди 4 — 6%. Сплавы с медью используются в производстве поршней двигателей внутреннего сгорания, высококачественных литых деталей летательных аппаратов.
Олово улучшает обработку резанием.
Титан. Основная задача титана в сплавах — измельчение зерна в отливках и слитках, что очень повышает прочность и равномерность свойств во всём объёме.
Алюминий — один из самых распространенных и дешевых металлов. Без него трудно представить себе современную жизнь. Недаром алюминий называют металлом 20 века. Он хорошо поддается обработке: ковке, штамповке, прокату, волочению, прессованию.
Чистый алюминий — довольно мягкий металл; из него делают электрические провода, детали конструкций, фольгу для пищевых продуктов, кухонную утварь и «серебряную» краску. Этот красивый и легкий металл широко используют в строительстве и авиационной технике. Алюминий очень хорошо отражает свет.
Поэтому его используют для изготовления зеркал — методом напыления металла в вакууме.
Источник: https://mirznanii.com/a/325500/svoystva-alyuminiya-i-oblasti-primeneniya-v-promyshlennosti-i-bytu
2.2.3. Характерные химические свойства алюминия
Алюминий — амфотерный металл. Электронная конфигурация атома алюминия 1s22s22p63s23p1. Таким образом, на внешнем электронном слое у него находятся три валентных электрона: 2 — на 3s- и 1 — на 3p-подуровне. В связи с таким строением для него характерны реакции, в результате которых атом алюминия теряет три электрона с внешнего уровня и приобретает степень окисления +3. Алюминий является высокоактивным металлом и проявляет очень сильные восстановительные свойства.
с кислородом
При контакте абсолютно чистого алюминия с воздухом атомы алюминия, находящиеся в поверхностном слое, мгновенно взаимодействуют с кислородом воздуха и образуют тончайшую, толщиной в несколько десятков атомарных слоев, прочную оксидную пленку состава Al2O3, которая защищает алюминий от дальнейшего окисления. Невозможно и окисление крупных образцов алюминия даже при очень высоких температурах. Тем не менее, мелкодисперсный порошок алюминия довольно легко сгорает в пламени горелки:
4Аl + 3О2 = 2Аl2О3
с галогенами
Алюминий очень энергично реагирует со всеми галогенами. Так, реакция между перемешанными порошками алюминия и йода протекает уже при комнатной температуре после добавления капли воды в качестве катализатора. Уравнение взаимодействия йода с алюминием:
2Al + 3I2 =2AlI3
С бромом, представляющим собой тёмно-бурую жидкость, алюминий также реагирует без нагревания. Образец алюминия достаточно просто внести в жидкий бром: тут же начинается бурная реакция с выделением большого количества тепла и света:
2Al + 3Br2 = 2AlBr3
Реакция между алюминием и хлором протекает при внесении нагретой алюминиевой фольги или мелкодисперсного порошка алюминия в заполненную хлором колбу. Алюминий эффектно сгорает в хлоре в соответствии с уравнением:
2Al + 3Cl2 = 2AlCl3
с серой
При нагревании до 150-200 оС или после поджигания смеси порошкообразных алюминия и серы между ними начинается интенсивная экзотермическая реакция с выделением света:
— сульфид алюминия
с азотом
При взаимодействии алюминия с азотом при температуре около 800 oC образуется нитрид алюминия:
с углеродом
При температуре около 2000oC алюминий взаимодействует с углеродом и образует карбид (метанид) алюминия, содержащий углерод в степени окисления -4, как в метане.
с водой
Как уже было сказано выше, стойкая и прочная оксидная пленка из Al2O3 не дает алюминию окисляться на воздухе. Эта же защитная оксидная пленка делает алюминий инертным и по отношению к воде. При снятии защитной оксидной пленки с поверхности такими методами, как обработка водными растворами щелочи, хлорида аммония или солей ртути (амальгирование), алюминий начинает энергично реагировать с водой с образованием гидроксида алюминия и газообразного водорода:
2Al + 6H2O = 2Al(OH)3 + 3H2
с оксидами металлов
После поджигания смеси алюминия с оксидами менее активных металлов (правее алюминия в ряду активности) начинается крайне бурная сильно-экзотермическая реакция. Так, в случае взаимодействия алюминия с оксидом железа (III) развивается температура 2500-3000оС. В результате этой реакции образуется высокочистое расплавленное железо:
2AI + Fe2O3 = 2Fe + Аl2О3
Данный метод получения металлов из их оксидов путем восстановления алюминием называется алюмотермией или алюминотермией.
с кислотами-неокислителями
Взаимодействие алюминия с кислотами-неокислителями, т.е. практически всеми кислотами, кроме концентрированной серной и азотной кислот, приводит к образованию соли алюминия соответствующей кислоты и газообразного водорода:
а) 2Аl + 3Н2SO4(разб.) = Аl2(SO4)3 + 3H2
2Аl0 + 6Н+ = 2Аl3+ + 3H20;
б) 2AI + 6HCl = 2AICl3 + 3H2
-концентрированной серной кислотой
Взаимодействие алюминия с концентрированной серной кислотой в обычных условиях, а также низких температурах не происходит вследствие эффекта, называемого пассивацией. При нагревании реакция возможна и приводит к образованию сульфата алюминия, воды и сероводорода, который образуется в результате восстановления серы, входящей в состав серной кислоты:
Такое глубокое восстановление серы со степени окисления +6 (в H2SO4) до степени окисления -2 (в H2S) происходит благодаря очень высокой восстановительной способности алюминия.
— концентрированной азотной кислотой
Концентрированная азотная кислота в обычных условиях также пассивирует алюминий, что делает возможным ее хранение в алюминиевых емкостях. Так же, как и в случае с концентрированной серной, взаимодействие алюминия с концентрированной азотной кислотой становится возможным при сильном нагревании, при этом преимущественно протекает реакция:
— разбавленной азотной кислотой
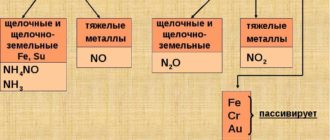
Взаимодействие алюминия с разбавленной по сравнению с концентрированной азотной кислотой приводит к продуктам более глубокого восстановления азота. Вместо NO в зависимости от степени разбавления могут образовываться N2O и NH4NO3:
8Al + 30HNO3(разб.) = 8Al(NO3)3 +3N2O + 15H2O
8Al + 30HNO3(оч. разб) = 8Al(NO3)3 + 3NH4NO3 + 9H2O
со щелочами
Алюминий реагирует как с водными растворами щелочей:
2Al + 2NaOH + 6H2O = 2Na[Al(OH)4] + 3H2
так и с чистыми щелочами при сплавлении:
В обоих случаях реакция начинается с растворения защитной пленки оксида алюминия:
Аl2О3 + 2NaOH + 3H2O = 2Na[Al(OH)4]
Аl2О3 + 2NaOH = 2NaAlO2 + Н2О
В случае водного раствора алюминий, очищенный от защитной оксидной пленки, начинает реагировать с водой по уравнению:
2Al + 6H2O = 2Al(OH)3 + 3H2
Образующийся гидроксид алюминия, будучи амфотерным, реагирует с водным раствором гидроксида натрия с образованием растворимого тетрагидроксоалюмината натрия:
Al(OH)3 + NaOH = Na[Al(OH)4]
Источник: https://scienceforyou.ru/teorija-dlja-podgotovki-k-egje/himicheskie-svojstva-aljuminija
Роль алюминия в организме человека. Источники, польза и вред
Алюминий входит в состав всех органов и систем человеческого организма. Он необходим для обеспечения большинства реакций, затрагивающих формирование белковых и фосфатных соединений.
Элемент также участвует и в других важных процессах, поэтому входит в набор незаменимых для человека витаминов и минералов. Но его поступление нужно контролировать, так как в больших концентрациях алюминий становится токсичным.
Значение и польза алюминия для человека
В сочетании с другими компонентами, алюминий поддерживает в нормальном состоянии следующие процессы:
- активная регенерация повреждённых клеток;
- формирование тканей опорно-двигательного аппарата и кожи;
- активация пищеварительных ферментов и желудочного сока;
- повышение чувствительности организма для усвоения белков;
- поддержание естественного цикла работы щитовидной железы.
Полезные свойства микроэлемента делают его незаменимой добавкой для людей с такими заболеваниями, как: остеопороз и переломы костей, язва, гастрит.
Симптомы недостатка микроэлемента
В медицинской практике случаев, когда обнаруживался дефицит алюминия в организме пациентов, практически не встречается. Это связано с его высокой усвояемостью и наличием во многих магазинных продуктах. Однако лабораторные исследования, проводимые на животных, установили возможные симптомы недостатка алюминия:
- ослабленные мышцы, кости и суставы;
- потеря двигательной активности, общая слабость;
- медленное восстановление при физических повреждениях;
- проблемы с координацией;
- выкидыши;
- ослабление когнитивных способностей.
Особое значение микроэлемент имеет для детей, чей организм развивается и нуждается в достаточном количестве алюминия. Если его поступает слишком мало, происходит задержка физического и умственного развития.
Недостаток алюминия развивается на фоне недостаточно богатого рациона: отсутствие овощей и фруктов, злаковых культур в меню, длительное потребление одной и той же пищи.
Избыток микроэлемента в организме очень опасен для здоровья.
При попадании в кровь, алюминий разносится по всем системам, поражая их. В большом количестве алюминий действует на клетки как канцерогенное вещество. Не давая им, делиться нормально. Клетки начинают беспорядочно размножаться, что может привести к серьезным осложнениям.
Причины и симптомы избытка элемента
Получить чрезмерное количество алюминия (свыше 50 мг) в сутки можно в следующих случаях:
- работа на производстве, связанном с использованием алюминиевых соединений;
- постоянное применение алюминиевой посуды без покрытия (ложки, тарелки и вилки), а также длительное хранение пищи в алюминиевых тарах, в том числе в тетра-паках с фольгой внутри;
- регулярное применение медицинских препаратов на основе алюминия;
- использование декоративной косметики с солями алюминия и другими соединениями, в которые входит молекула металла;
- наличие острой почечной недостаточности – при заболевании происходит сбой, и в организме усиливается накопление солей элемента;
- чрезмерное употребление продуктов с повышенным содержанием микроэлемента;
- употребление магазинных полуфабрикатов и некоторых фабричных блюд с консервантами (сульфаты и соли алюминия: Е520, Е521, Е522, Е523);
- регулярное питье воды, богатой алюминиевыми соединениями.
Точно определить, в каком именно городе риск отравиться алюминием выше, невозможно. Однако существуют территории, на которых люди получают гораздо больше минерала, вдыхая его вместе с воздухом (места, где расположены заводы по переработке алюминия и другие металлургические предприятия).
Симптомы избытка микроэлемента
Чрезмерное употребление соединений алюминия вместе с пищей вызывает такие состояния, как:
- умеренный и сильный кашель,
- потеря аппетита,
- повышенная нервозность,
- проблемы с пищеварением,
- дезориентация,
- заболевания почек.
У людей с повышенной концентрацией металла в крови отмечается снижение количества эритроцитов и уровня гемоглобина.
При длительном накоплении алюминия в организме возможны провалы в памяти, депрессии, развитие болезни Альцгеймера в зрелом возрасте. При острой интоксикации в течение долгого времени могут возникнуть тяжёлые нарушения:
- судороги и конвульсии, артрит и рахит;
- размягчение костной ткани и последующие проблемы с опорно-двигательным аппаратом, постоянные переломы;
- энцефалопатии, проявляющиеся психическими проблемами и депрессиями;
- острые нарушения со стороны ЦНС;
- недостаточный уровень магния, меди, цинка, железа, кальция и фосфора.
Алюминий угнетает активность иммунной системы, и постоянное воздействие высоких доз на организм сильно сокращает продолжительность жизни человека.
Алюминий в продуктах питания
С водой и пищей человек каждый день получает довольно высокие дозы алюминия, но усваивается из них не более 4%. Вода обогащается алюминием в местах, где очищение реализуют с помощью алюмокалиевых квасцов. Повышенный уровень минерала в жидкости встречается и там, где регулярно идут кислотные дожди.
В растительной пище минерала содержится в несколько раз больше, чем в мясе и продуктах животного происхождения. Дополнительным источником алюминия служит посуда из этого металла, особенно не покрытая защитными веществами. Под действием температуры металл из фольги, посуды, столовых приборов может переходить в обрабатываемую пищу. А вот в еде он не разрушается.
Факт! В состав дрожжей входят соединения алюминия. В сочетании с формами, используемыми для выпечки, этот фактор повышает концентрацию металла в хлебе в несколько раз.
Плавленый сыр – отдельный продукт, при производстве которого используются химические плавители. В их состав входят соединения алюминия. Усиленные консервантами, они повышают содержание микроэлемента в сыре, несмотря на то, что он относится к продуктам животного происхождения.
Растительные источники алюминия:
- меньше всего содержится в яблоках и чечевице – от 0,11 до 0,17 мг;
- в огурцах, винограде и моркови – от 0,323 до 0,42 мг;
- в кукурузе, капусте, манке – от 0,425 до 0,57 мг;
- в фасоли, персиках, киви, савойской капусте, баклажанах, авокадо, топинамбуре – от 0,6 до 0,815 мг;
- в картофеле и рисе – от 0,86 до 0,91 мг;
- в муке высшего, 1 и 2 сорта содержится 1,05-1,4 мг;
- больше всего алюминия содержит рожь, пшеница и сорго – от 1,5 до 1,67 мг;
Особое внимание люди должны обращать на хлеб, покупаемый в магазинах. Даже если это суперполезный серый батон с отрубями, в его составе будет запредельное количество алюминия. И отсутствие дрожжей не компенсирует этот фактор. Таким образом, увлекаться любой выпечкой не рекомендуется никому. Даже если человек не соблюдает низкокалорийную диету.
Взаимодействие с другими элементами
При использовании алюминиевой посуды нужно помнить, что выделение ионов металла активируется при взаимодействии незащищённой поверхности с кислотами (лимонный сок, уксус, любые цитрусы).
Важно! Алюминиевые соединения, поступающие в больших количествах, блокируют усвоение витамина C, серосодержащих аминокислот, витамина B6, кальция, железа и магния.
Ухудшается усвоение фосфора, если в рационе постоянно присутствуют большие дозы алюминия. При этом магний способен нейтрализовать соединения металла, аналогичными свойствами обладают ионы серебра, железа, кальция и меди.
Норма суточного потребления
Точных исследований, устанавливающих норму для разных возрастов, не существует. Но известно, что потребление меньше, чем 0,001 мг алюминия в сутки, может привести к дефициту микроэлемента. Критической считается дозировка в 50 мг. Из-за распространённости алюминия в промышленности контролировать сложнее не недостаток, а избыток элемента.
Передозировка металлом не проявляется сразу же, для этого в организме должно накопиться много запасов алюминия. Поэтому последствия интоксикации наблюдаются лишь спустя несколько лет после того, как человек начал регулярно получать большие дозы металла (с пищей, водой или воздухом).
Влияние алюминия на беременность
Исследований на людях относительно воздействия алюминия на плод и беременную женщину не проводилось. Но лабораторные испытания на животных позволили установить, что высокие дозировки металла приводят к его накоплению в тканях плода. А это чревато многими нарушениями:
- задержка развития эмбриона;
- медленное формирование скелета;
- пороки развития органов и систем;
- невынашивание;
- внутриутробная смерть.
Новорожденные отличаются высокой чувствительностью к алюминию, поэтому потенциально матери запрещено принимать средства от гастрита, язвы, другие препараты с алюминием.
Алюминий в медицине и косметологии
Соединения металла используются в медицине давно – первые упоминания отслеживаются с XV столетия. В то время алюминиевые квасцы использовали славяне для заживления кожных ран. Алюминиевые соединения широко используются в производстве дезодорантов: эти вещества закупоривают поры, но в виде солей способны откладываться в организме.
Факт! Встретить металл можно в составе влажных салфеток и полотенец.
Самые популярные лекарства с высоким содержанием алюминия – это препараты от гастрита, язвы и изжоги («Алюмаг», «Алмагель», «Антацид», «Гастал», «Алюгастрин»). Таблетки, упакованные в блистеры и соприкасающиеся с алюминиевой фольгой, могут иметь следы ионов металла в составе.
Алюминий – микроэлемент, который не возглавляет списки витаминов и минералов, необходимых для здоровья человека. Но в низких дозировках он полезен для организма.
Однако для их получения нет нужды употреблять специальные добавки или вводить в рацион продукты с высоким содержанием металла.
Наоборот, чаще всего приходится ограничивать его поступление – пищевая промышленность позаботилась о том, чтобы вместе с полуфабрикатами и консервами человек получал большие дозы минерала.
Источник: https://polzaili.ru/rol-alyuminiya-v-organizme-cheloveka-istochniki-polza-i-vred/
Как настроить Айфон 11 после покупки — инструкция
Помогаем разобраться с Айфоном 11. Плюсы и минусы смартфона, новые фишки. Как настроить телефон.
Сильные и слабые стороны iPhone 11 приведены в таблице:
| Преимущества | Недостатки |
| Улучшенный дисплей у моделей Pro и Pro Max. Известная и полюбившаяся всем матрица OLED модернизирована: добавлена поддержка форматов HDR и поднята контрастность. Благодаря усовершенствованиям изображение яркое и в то же время не «режет» глаз, а также не тускнеет даже под влиянием прямых солнечных лучей. | Незначительный объем интегрированной памяти. Многие компании, в том числе китайские, подняли минимальный показатель встроенного накопителя до 128 Гб и выше, а у Apple он так и остался равным 68 Гб. Причем докупить и разместить съемную карту памяти невозможно — для нее не предусмотрено места. |
| Увеличенная производительность. Она обеспечивается мощнейшим процессором A13 Bionic, пересмотренной системой машинного обучения и трехмодульной камерой. | Экономия на USB-C. Несмотря на ожидания после выхода iPad Pro, быструю зарядку так и не положили в коробку к iPhone, хоть он и совместим с ней. Ее стоимость превышает 5 тысяч рублей. |
| Более быстрый графический процессор. Он на двадцать процентов продуктивнее, чем прошлый. | Отсутствие реверсивной подзарядки. Практически все аналитики были уверены в том, что после обновления Samsung Galaxy, «Эппл» не захочет отставать от главного конкурента и тоже внедрит технологию «подпитки» других гаджетов от смартфона. Но, к сожалению, этого не произошло. |
| Более продолжительная работа в автономном режиме. Она гарантируется аккумулятором емкостью более 3 тысяч мАч и достигла отметки в 86 часов, что на 4 часа дольше. | |
| Более современная защита от воды и пыли. iPhone 11 сохраняет свою функциональность при погружении в воду до двух метров на тридцать минут, так как в нем использован стандарт IP68. В предыдущих моделях задействовались менее серьезные нормы IP67. |
Отдельно следует остановиться на новых «фишках» Айфон 11. К ним относится:
- Новые цвета. Ценители Apple могут выбрать iPhone 11 в одном из оттенков: белом, черном, красном, желтом, зеленом и фиолетовом.
- 3D-стекло. Корпус айфона 11 изготовлен из анодированного алюминия, который будто «перетекает» в 3D-стекло, что создает потрясающий визуальный эффект.
- Большее число камер. У iPhone 11 их две, а у моделей Pro и Pro Max их три. Основная камера двенадцатимегапиксельная, с несколькими режимами съемки и автофокусировкой и другими опциями. Дополнительная камера оснащена сверхширокоугольным объективом, позволяющим почувствовать себя настоящим кинематографистом.
- Замедленное селфи. На Айфоне 11 возможно сделать слоумо. Для этого необходимо зайти в «Камеру», переключиться на фронтальную камеру и перейти в режим замедленного селфи. Дальше остается только проявлять фантазию.
- Детализированные фотографии. iPhone 11 формирует четыре основных и четыре дополнительных изображения еще до того, как вы дотронетесь до затвора. В результате снимок получается прорисованным «пиксель за пикселем».
- Ночной режим. С айфоном 11 вам удастся добиться красивых фотографий даже в том случае, если вокруг темно. Ночной режим начинает активируется самостоятельно и не требует включения вспышки. С изображения убираются участки с размытостью и шумами. Кроме того, снимок детализируется.
- Корректировка силы звука. Предположим, что вы снимаете человека, который что-то говорит. Его голос будет более громким, чем все остальное (объявления, доносящиеся из магазинов, шум, издаваемый спецтехникой и т.д.).
- Воспроизведение музыки по технологии объемного звука. Динамики работают на основе пространственного аудио.
- Поддержка Wi-Fi 6. Одиннадцатый айфон стал первым смартфоном с поддержкой Wi-Fi 6. Это значит, что выросла скорость Интернета.
Первый запуск смартфона
Для первого запуска устройства необходимо нажать всего лишь на одну кнопку — ту, которая находится сбоку. Держите палец на ней до тех пор, пока не появится фирменный логотип компании Apple и приветствие на самых популярных языках мира. Следуйте инструкции.
Если вы очень плохо видите, то воспользуйтесь функцией VoiceOver или «Увеличение».
Вам будет предложено несколько языков. Выберите один из них.
Также потребуется определиться со страной и более конкретным местоположением. Указывайте актуальное местоположение, так как от него зависит показ даты, времени, контактов и др.
Активация и настройка Айфона 11
Активация Айфона 11 может быть произведена через:
- Wi-Fi.
- Мобильную сеть.
- iTunes.
Предварительно нужно вставить SIM-карту. Допускается использовать как уже действующую, так и новую.
Что касается настройки Айфона 11, то ее лучше всего осуществлять через «Быстрое начало». Правда, есть одно «но»: этот способ подходит только для тех, кто имеет iPhone или iPad предыдущей модели. Процесс выглядит так:
- Вставляете в новое устройство сим-карту. Доставать ее удобно специальным приспособлением, идущим в комплекте, но справиться с задачей возможно и при помощи обычной скрепки небольшого размера.
- Включаете оба мобильных телефона и кладете их рядом друг с другом. И на первом, и на втором должна быть установлена операционная система iOS не ниже одиннадцатой версии.
- Замечаете надпись «Быстрое начало» на старом устройстве, после чего проверяете идентификатор и клацаете по слову «Продолжить». Если надписи «Быстрое начало» на старом устройстве нет, то проблема или в невключенном Bluetooth, или в устаревшей iOS.
- Дожидаетесь анимации на новом мобильном телефоне и проводите автоматическую (посредством видоискателя) или ручную аутентификацию.
- Сообщаете код-пароль от старого устройства в новом мобильном телефоне.
- Вводите Apple ID в новом устройстве.
На настройку iPhone 11 уходит от двух минут до нескольких часов в зависимости от объема данных и скорости выхода в Интернет.
Не забывайте о том, что при синхронизации нельзя блокировать доступ в Интернет и отключать зарядки.
Более подробно о настройке iPhone 11 рассказано в видео
Как создать Apple ID
Источник: https://tarifkin.ru/mobilnye-sovety/kak-polzovatsya-ajfonom-11